解答题-原理综合题 适中0.65 引用1 组卷156
回答下列问题:
(1)某研究性学习小组利用Na2S2O3溶液和稀硫酸溶液的反应生成单质硫和二氧化硫,探究浓度和温度对化学反应速率的影响,进行了如下实验:
①写出该反应的离子方程式:_______ 。
②V1 =_______ 、T1 = _______ ;V2 = _______ 。
③实验A、B两个实验对比,可以研究的问题是:_______
(2)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
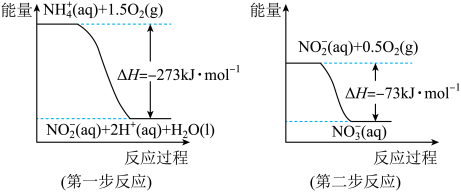
1 mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(3)有人用图3进行H2O2与MnO2反应的速率测定实验。
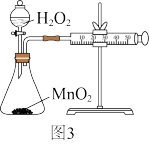
①有人认为可将装置改进为图4,你认为是否合理_______ (选填“合理”或“不合理”)。
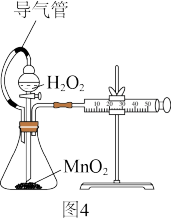
②实验中,加入10ml 2mol/L的H2O2,反应10s时,收集到22.4mL氧气,则这10s内,用过氧化氢表示的反应速率是_______ mol/(L·s)。
(1)某研究性学习小组利用Na2S2O3溶液和稀硫酸溶液的反应生成单质硫和二氧化硫,探究浓度和温度对化学反应速率的影响,进行了如下实验:
| 实验序号 | 实验温度/K | 有关物质 | 浑浊所需时间/s | ||||
| 稀硫酸溶液 | Na2S2O3溶液 | H2O | |||||
| V/mL | c/mol·L–1 | V/mL | c/mol·L–1 | V/mL | |||
| A | 298 | 2 | 0.1 | 5 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.1 | 4 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.1 | V2 | 0.1 | 1 | t2 |
②V1 =
③实验A、B两个实验对比,可以研究的问题是:
(2)在微生物作用的条件下,NH

1 mol NH
(3)有人用图3进行H2O2与MnO2反应的速率测定实验。

①有人认为可将装置改进为图4,你认为是否合理

②实验中,加入10ml 2mol/L的H2O2,反应10s时,收集到22.4mL氧气,则这10s内,用过氧化氢表示的反应速率是
21-22高二上·广东深圳·期中
类题推荐
I.如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图像回答问题:
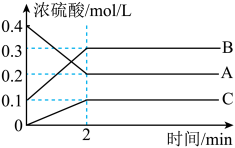
(1)2min内,用C表示的反应速率为______________ 。
(2)该反应的方程式为______________ 。
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,________ 。
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
(4)通过实验A、B,可探究出___________ (填外部因素)的改变对化学反应速率的影响,其中V1=_____ 、T1=_____ ;通过实验________ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=_______ ,t2_______ 8 (填写“=”、“>”或“<”)。
(5)若t1<8,则由此实验可以得出的结论是_______ 。

(1)2min内,用C表示的反应速率为
(2)该反应的方程式为
(3)在其他条件下,测得A的反应速率为0.05 mol/(L·s),此时的反应与800℃时相比,
A.比800℃ 时快 B.比800℃ 时慢 C.和800℃ 时速率一样
Ⅱ.学习小组甲利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如表实验:
实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(5)若t1<8,则由此实验可以得出的结论是
回答下列问题:
(1)某研究性学习小组利用Na2S2O3溶液和稀硫酸溶液的反应探究浓度和温度对化学反应速率的影响,进行了如下实验:
①写出该反应的离子方程式:_______ 。
②V1=_______ 、T1=_______ ;V2=_______ 。
(2)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
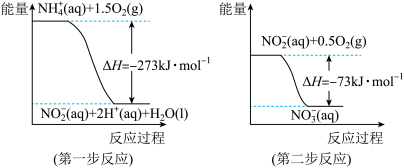
1mol (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(3)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表所示:
①该反应为_______ 反应(填“吸热”或“放热”)。
②某温度下,平衡浓度符合下式:c(CO2)∙c(H2)=c(CO)∙c(H2O),试判断此时的温度为_______ ℃。
③在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol/L,c(H2)=1.5mol/L,c(CO)=1mol/L,c(H2O)=3mol/L,则下一时刻,反应向_______ (填“正向”或“逆向”)进行。
(1)某研究性学习小组利用Na2S2O3溶液和稀硫酸溶液的反应探究浓度和温度对化学反应速率的影响,进行了如下实验:
| 实验序号 | 实验温度/K | 有关物质 | 浑浊所需时间/s | ||||
| 稀硫酸溶液 | Na2S2O3溶液 | H2O | |||||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
| A | 298 | 2 | 0.1 | 5 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.1 | 4 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.1 | V2 | 0.1 | 1 | t2 |
①写出该反应的离子方程式:
②V1=
(2)在微生物作用的条件下,

1mol
(3)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表所示:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应为
②某温度下,平衡浓度符合下式:c(CO2)∙c(H2)=c(CO)∙c(H2O),试判断此时的温度为
③在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2mol/L,c(H2)=1.5mol/L,c(CO)=1mol/L,c(H2O)=3mol/L,则下一时刻,反应向
某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)写出草酸与高锰酸钾反应的离子方程式___________ 。
(2)通过实验A、B,可探究出___________ (填外部因素)的改变对化学反应速率的影响,其中V1=___________ 、T1=___________ ;通过实验___________ (填实验序号)可探究出温度变化对化学反应速率的影响
(3)忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率
___________ 。
| 实验序号 | 实验温度 | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 和酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/ mol·L-1 | V/mL | c/ mol·L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)通过实验A、B,可探究出
(3)忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


