解答题-结构与性质 0.4 引用2 组卷279
铬是一种重要的战略金属元素,在工业生产中有着重要的应用。
(1)基态铬原子的价层电子排布式为_______ 。
(2)金属铬的第二电离能 和锰的第二电离能
和锰的第二电离能 分别为
分别为 、
、 ,
, 的原因是
的原因是_______ 。
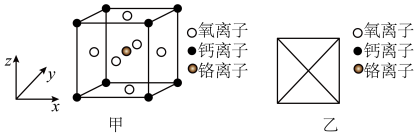
(3)铬、钙、氧可形成一种具有特殊导电性的复合氧化物,其晶胞结构如图甲所示。_______ 。
②请在图乙中画出该晶胞沿 轴方向的投影图
轴方向的投影图_______ 。
③已知氧离子与钙离子的最近距离为 ,请计算该晶体的密度:
,请计算该晶体的密度:_______  (列计算式)。
(列计算式)。
(4)三氯化铬晶体 是一种难溶于乙醚,易溶于水、乙醇的绿色晶体,可作为猪饲料的添加剂。某研究小组以铬酸钠
是一种难溶于乙醚,易溶于水、乙醇的绿色晶体,可作为猪饲料的添加剂。某研究小组以铬酸钠 为主要原料制备
为主要原料制备 ,实验步骤如下:
,实验步骤如下:
i、将铬酸钠、甲醇、水依次加入三颈烧瓶中;
ii、升温至 ,加入过量盐酸,保持温度在
,加入过量盐酸,保持温度在 继续反应三小时;
继续反应三小时;
iii、待反应液冷却后,用 溶液调节
溶液调节 ,得到
,得到 沉淀;
沉淀;
iv、_______,得到 晶体。
晶体。
①下列说法正确的是_______ (填序号)。
A由于步骤i中的甲醇具有毒性,故可用乙醇代替
B.步骤ii应快速加入过量盐酸,防止 水解而导致反应液出现浑浊
水解而导致反应液出现浑浊
C.三颈烧瓶中发生反应的离子方程式为
D.制备过程中应采用水浴加热,以便于控制温度
②步骤iv的实验操作如下:将过滤得到的固体溶于足量的盐酸中,_______ ,用_______ 洗涤,干燥后得到 晶体。
晶体。
(1)基态铬原子的价层电子排布式为
(2)金属铬的第二电离能
(3)铬、钙、氧可形成一种具有特殊导电性的复合氧化物,其晶胞结构如图甲所示。
②请在图乙中画出该晶胞沿
③已知氧离子与钙离子的最近距离为
(4)三氯化铬晶体
i、将铬酸钠、甲醇、水依次加入三颈烧瓶中;
ii、升温至
iii、待反应液冷却后,用
iv、_______,得到
①下列说法正确的是
A由于步骤i中的甲醇具有毒性,故可用乙醇代替
B.步骤ii应快速加入过量盐酸,防止
C.三颈烧瓶中发生反应的离子方程式为
D.制备过程中应采用水浴加热,以便于控制温度
②步骤iv的实验操作如下:将过滤得到的固体溶于足量的盐酸中,
2022·浙江·模拟预测


