填空题 适中0.65 引用1 组卷85
按要求填空:
(1)13gC2H2(g)完全燃烧生成CO2(g)和H2O(l)时,放出659kJ的热量,写出该反应的热化学方程式_____ 。
(2)试写出镁粉投入NH4Cl溶液中反应的离子方程式_____ 。
(3)AlCl3水溶液的pH值_____ 7(填“>”、“<”或“=”),原因是(用离子方程式表示)______ 。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_____ 。
(4)在配制Na2S溶液时,为了防止发生水解,可以加入少量的_____ 。
(5)常温下,测得CH3COONH4溶液的pH=7,则说明CH3COO-的水解程度______ (填“>”、“<”或“=”)NH 的水解程度,CH3COO-与NH
的水解程度,CH3COO-与NH 浓度的大小关系是:c(CH3COO-)
浓度的大小关系是:c(CH3COO-)______ c(NH )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
(1)13gC2H2(g)完全燃烧生成CO2(g)和H2O(l)时,放出659kJ的热量,写出该反应的热化学方程式
(2)试写出镁粉投入NH4Cl溶液中反应的离子方程式
(3)AlCl3水溶液的pH值
(4)在配制Na2S溶液时,为了防止发生水解,可以加入少量的
(5)常温下,测得CH3COONH4溶液的pH=7,则说明CH3COO-的水解程度
21-22高二上·黑龙江牡丹江·阶段练习
类题推荐
按要求完成下列问题。
(1)已知NH4Cl水溶液呈酸性。
①NH4Cl水溶液呈酸性的原因_______ (用离子方程式解释)。
②在NH4Cl水溶液中各离子浓度的大小关系是_______ 。
③常温下,pH=4的NH4Cl溶液中,水电离出c(H+)=_______ 。
④常温下,pH=7的NH4Cl和NH3·H2O的混合液中c( )
)_______ c(Cl-)(填>、<或=)。
(2)实验室在配制AlCl3的溶液时,为了抑制AlCl3的水解可加入少量的_______ (填写物质的名称)。把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是_______ (填化学式)。实验室配制0.001mol/LAlCl3溶液时,为了抑制AlCl3的水解使溶液中不产生沉淀,需要调整溶液的pH不大于_______ [Al(OH)3的Ksp=1.0×10-33]。
(3)毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用重石制备BaCl2·2H2O的流程如图:
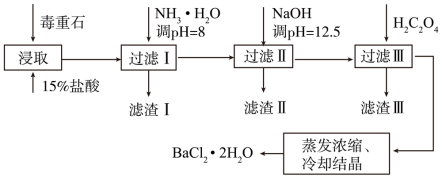
已知:
Ksp(BaC2O4)=1.6×10−7,Ksp(CaC2O4)=2.3×10−9。
加入NH3·H2O调pH=8可除去_______ (填离子符号),滤渣II中含_______ (填化学式)。加入H2C2O4时应避免过量,原因是_______ 。
(1)已知NH4Cl水溶液呈酸性。
①NH4Cl水溶液呈酸性的原因
②在NH4Cl水溶液中各离子浓度的大小关系是
③常温下,pH=4的NH4Cl溶液中,水电离出c(H+)=
④常温下,pH=7的NH4Cl和NH3·H2O的混合液中c(
(2)实验室在配制AlCl3的溶液时,为了抑制AlCl3的水解可加入少量的
(3)毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用重石制备BaCl2·2H2O的流程如图:

已知:
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
Ksp(BaC2O4)=1.6×10−7,Ksp(CaC2O4)=2.3×10−9。
加入NH3·H2O调pH=8可除去
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


