解答题-实验探究题 较难0.4 引用2 组卷244
探究化学反应速率的影响因素,对工农业生产有着非常重要的意义。为探究反应速率与 溶液浓度的关系,利用下列装置(夹持仪器略去)进行实验。
溶液浓度的关系,利用下列装置(夹持仪器略去)进行实验。
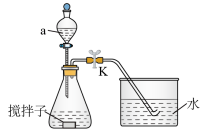
实验步骤:往锥形瓶中加入一定体积的
 溶液、
溶液、
 溶液和水,充分搅拌。控制体系温度,通过
溶液和水,充分搅拌。控制体系温度,通过 往锥形瓶中加入一定浓度的醋酸,发生反应:
往锥形瓶中加入一定浓度的醋酸,发生反应: 。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集
。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集
 所需时间。回答下列问题:
所需时间。回答下列问题:
(1)仪器a的名称为_______ 。
(2)若需控制体系的温度为36℃,采取的合理加热方式为_______ 。
(3)每组实验过程的实验数据如下表所示:
i.
_______ ,
_______ 。
ii.该反应的速率方程为 ,k为反应速率常数。利用实验数据计算得m=
,k为反应速率常数。利用实验数据计算得m=_______ (填整数)。
iii.醋酸的作用是_______ 。
(4)如果用同浓度的盐酸代替醋酸进行实验1, 与盐酸反应生成
与盐酸反应生成 ,
, 分解产生等物质的量的两种气体。反应结束后,锥形瓶中红棕色气体逐渐变浅。
分解产生等物质的量的两种气体。反应结束后,锥形瓶中红棕色气体逐渐变浅。 分解的化学方程式为
分解的化学方程式为_______ 。

实验步骤:往锥形瓶中加入一定体积的
(1)仪器a的名称为
(2)若需控制体系的温度为36℃,采取的合理加热方式为
(3)每组实验过程的实验数据如下表所示:
| 实验编号 | |||||
| 醋酸 | 水 | ||||
| 1 | 4.0 | 4.0 | 8.0 | 340 | |
| 2 | 6.0 | 4.0 | 4.0 | 151 | |
| 3 | 8.0 | 4.0 | 4.0 | 4.0 | 85 |
| 4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
ii.该反应的速率方程为
iii.醋酸的作用是
(4)如果用同浓度的盐酸代替醋酸进行实验1,
22-23高二上·山东滨州·期中
类题推荐  溶液和
溶液和 溶液可发生反应:
溶液可发生反应: 。为探究反应速率与
。为探究反应速率与 的关系,利用图装置(夹持仪器略去)进行实验。
的关系,利用图装置(夹持仪器略去)进行实验。
实验步骤:往A中加入VmL的 溶液、
溶液、 溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入
溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入 醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集
醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集 所需的时间,重复多次取平均值(t)。
所需的时间,重复多次取平均值(t)。
回答下列问题:

(1)仪器A的名称为_______ 。
(2)检验装置气密性的方法:关闭止水夹K,_______ 。
(3)若需控制体系的温度为36℃,采取的合理加热方式为_______ 。
(4)每组实验过程中,反应物浓度变化很小,忽路其对反应速率测定的影响。实验数据如表所示。
①
_______ ,
_______ 。
②该反应的速率方程为 、k为反应速率常数,利用实验数据计算得m=
、k为反应速率常数,利用实验数据计算得m=_______ (填整数)。
③醋酸的作用是_______ 。
实验步骤:往A中加入VmL的
回答下列问题:

(1)仪器A的名称为
(2)检验装置气密性的方法:关闭止水夹K,
(3)若需控制体系的温度为36℃,采取的合理加热方式为
(4)每组实验过程中,反应物浓度变化很小,忽路其对反应速率测定的影响。实验数据如表所示。
| 实验编号 | V/mL | t/s | |||
| 醋酸 | 水 | ||||
| 1 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
| 2 | 8.0 | 4.0 | 4.0 | 83 | |
| 3 | 4.0 | 4.0 | 150 | ||
| 4 | 4.0 | 4.0 | 8.0 | 334 | |
②该反应的速率方程为
③醋酸的作用是
请回答下列问题:
(一)一定温度下,向2L恒容密闭容器中充入0.40mol无色气体 ,发生反应:
,发生反应: ,一段时间后达到平衡,测得数据如下:
,一段时间后达到平衡,测得数据如下:
(1)0-40s内,
___________  。
。
(2)0-20s,气体颜色加深,此时 余下的物质的量为
余下的物质的量为___________ mol;此时 的分解率为
的分解率为___________ 。
(二) 溶液和
溶液和 溶液可发生反应:
溶液可发生反应: 。为探究反应速率与
。为探究反应速率与 的关系,利用下列装置(夹持仪器略去)进行实验。
的关系,利用下列装置(夹持仪器略去)进行实验。
实验步骤:往A中加入一定体积(V)的 溶液、
溶液、 溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0mol/L醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集
溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0mol/L醋酸。当导管口气泡均匀稳定冒出时,开始用排水法收集气体。用秒表测量收集 所需的时间,重复多次取平均值(t)。回答下列问题:
所需的时间,重复多次取平均值(t)。回答下列问题:
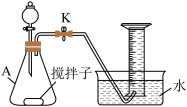
(3)仪器A的名称为___________ 。
(4)若需控制体系的温度为36℃,采取的合理加热方式为___________ 。
(5)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如下表所示。
①
___________ ,
___________ 。
②该反应的速率方程为 ,k为反应速率常数。利用实验数据计算得
,k为反应速率常数。利用实验数据计算得
___________ (填整数)。
③醋酸的作用是___________ 。
(一)一定温度下,向2L恒容密闭容器中充入0.40mol无色气体
| 时间/s | 20 | 40 | 60 | 80 | 100 |
| 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
(2)0-20s,气体颜色加深,此时
(二)
实验步骤:往A中加入一定体积(V)的

(3)仪器A的名称为
(4)若需控制体系的温度为36℃,采取的合理加热方式为
(5)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如下表所示。
| 实验编号 | |||||
| 醋酸 | 水 | ||||
| 1 | 4.0 | 4.0 | 8.0 | 334 | |
| 2 | 4.0 | 4.0 | 150 | ||
| 3 | 8.0 | 4.0 | 4.0 | 4.0 | 83 |
| 4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
②该反应的速率方程为
③醋酸的作用是
NaNO2溶液和NH4Cl溶液可发生反应:NaNO2+NH4Cl N2+NaCl+2H2O。为探究反应速率与c(NaNO2)的关系,利用下列装置(夹持仪器略去)进行实验。
N2+NaCl+2H2O。为探究反应速率与c(NaNO2)的关系,利用下列装置(夹持仪器略去)进行实验。
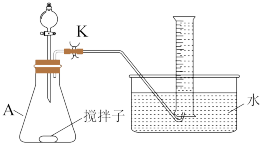
实验步骤:往A中加入一定体积(V)的2.0mol·L-1NaNO2溶液、2.0mol·L-1NH4Cl溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0mol·L-1醋酸。当导件口气泡均匀稳定冒出时,开始用排水法收集气体。用种表测量收集1.0mLN2所需时间,重复多次取平均值(t)。
回答下列问题:
(1)仪器A的名称为_______ 。
(2)检验装置气密性的方法:关闭止水夹K,_______ 。
(3)若需控制体系的温度为36℃,采取的合理加热方式为_______ 。
(4)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如下表所示。
①V1=_______ ,V3=_______ 。
②该反应的速率方程为v=k·cm(NaNO2)·c(NH4Cl)·c(H+),k为反应速率常数。利用实验数据计算得m=_______ (填整数)。

实验步骤:往A中加入一定体积(V)的2.0mol·L-1NaNO2溶液、2.0mol·L-1NH4Cl溶液和水,充分搅拌。控制体系温度,通过分液漏斗往A中加入1.0mol·L-1醋酸。当导件口气泡均匀稳定冒出时,开始用排水法收集气体。用种表测量收集1.0mLN2所需时间,重复多次取平均值(t)。
回答下列问题:
(1)仪器A的名称为
(2)检验装置气密性的方法:关闭止水夹K,
(3)若需控制体系的温度为36℃,采取的合理加热方式为
(4)每组实验过程中,反应物浓度变化很小,忽略其对反应速率测定的影响。实验数据如下表所示。
| 实验编号 | V/mL | t/s | |||
| NaNO2溶液 | NH4Cl溶液 | 醋酸 | 水 | ||
| 1 | 4.0 | V1 | 4.0 | 8.0 | 334 |
| 2 | V2 | 4.0 | 4.0 | V3 | 150 |
| 3 | 8.0 | 4.0 | 4.0 | 4.0 | 83 |
| 4 | 12.0 | 4.0 | 4.0 | 0.0 | 38 |
②该反应的速率方程为v=k·cm(NaNO2)·c(NH4Cl)·c(H+),k为反应速率常数。利用实验数据计算得m=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


