填空题 较难0.4 引用2 组卷114
硫酸酸化的高锰酸钾溶液与草酸发生化学反应,反应如下:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,某化学兴趣小组为了测定草酸浓度,主要做了如下实验。用0.1000mol/L酸性高锰酸钾溶液滴定未知浓度的H2C2O4溶液。实验中测得的数据记录如下:
请回答:
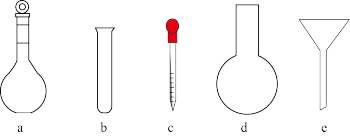
(1)配制KMnO4标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要图中的______ (填字母代号)。
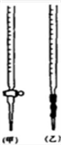
(2)用配制好的高锰酸钾滴定草酸时,高锰酸钾溶液应盛装于_______ (如图,填“甲”或“乙”)滴定管。滴定时,眼睛应注视______________________ 。

(3)该实验中未使用指示剂就可判断终点,到达终点的判断标志是____________ 。
(4)根据表中数据,计算H2C2O4溶液的浓度______________ 。
(5)下列造成H2C2O4溶液的浓度偏高的是_________________________________。
| 滴定次数 | H2C2O4体积 | 滴定前KMnO4体积 | 终点时KMnO4体积 |
1 | 25.00mL | 0.00mL | 21.41mL |
2 | 25.00mL | 0.02mL | 21.44mL |
3 | 25.00mL | 1.04mL | 22.47mL |
4 | 25.00mL | 0.04mL | 24.46 mL |
(1)配制KMnO4标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要图中的

(2)用配制好的高锰酸钾滴定草酸时,高锰酸钾溶液应盛装于

(3)该实验中未使用指示剂就可判断终点,到达终点的判断标志是
(4)根据表中数据,计算H2C2O4溶液的浓度
(5)下列造成H2C2O4溶液的浓度偏高的是_________________________________。
| A.滴定终点读数时俯视 | B.滴定前有气泡,滴定后气泡消失 |
| C.润洗锥形瓶 | D.滴定过程中加入少量蒸馏水冲洗瓶壁 |
21-22高二上·内蒙古赤峰·期中
类题推荐
滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)酸碱中和滴定——用浓度为 的标准盐酸滴定未知浓度的NaOH溶液,表格中记录了实验数据:
的标准盐酸滴定未知浓度的NaOH溶液,表格中记录了实验数据:
①配置实验用的标准盐酸240 mL,需要用到的玻璃仪器有移液管、烧杯、玻璃棒、___________ 、___________ 。
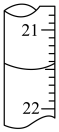
②图中的滴定管读数为___________ mL;通过该实验测得NaOH溶液的物质的量浓度为___________ mol/L。(小数点后保留四位有效数字)
③下列操作造成测定结果偏低的是___________ (填选项字母)。
A.滴定终点读数时,俯视滴定管刻度,其他操作正确
B.盛装待测液的锥形瓶洗涤后还残留有蒸馏水
C.碱式滴定管用蒸馏水洗净后,未用待测液润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取一定量的草酸(H2C2O4)溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时KMnO4溶液应装在___________ (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是___________ ;该反应的离子方程式为___________ 。
(1)酸碱中和滴定——用浓度为
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.50 | 20.40 |
| 第二次 | 20.00 | 3.00 | 23.00 |
| 第三次 | 20.00 | 4.00 | 24.10 |
②图中的滴定管读数为

③下列操作造成测定结果偏低的是
A.滴定终点读数时,俯视滴定管刻度,其他操作正确
B.盛装待测液的锥形瓶洗涤后还残留有蒸馏水
C.碱式滴定管用蒸馏水洗净后,未用待测液润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取一定量的草酸(H2C2O4)溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时KMnO4溶液应装在
草酸晶体的组成可表示为:H2C2O4·XH2O,为测定X值,进行下列实验:
①称取wg草酸晶体配成100.00mL水溶液;
②用移液管取25.00mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为cmol·L-1KMnO4滴定。滴定时,所发生的反应化学方程式为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
请回答下列问题:
(1)实验①中为配制准确物质的量浓度的草酸溶液,所需用到的仪器是:天平(含砝码)、烧杯、药匙、玻璃棒和____ 。
(2)实验②中,滴定时,KMnO4溶液应装在____ (填“酸式滴定管”或“碱式滴定管”)中。
(3)滴定中,双眼应注视____ ,判断滴定终点的标准是____ 。
(4)若滴定是准确的,反应前后的两次读数分别为a和b,则实验测得所配草酸溶液的物质的量浓度为____ 。
(5)下列操作,会导致草酸的物质的量浓度偏高的是____ (填序号)。
①称取wg草酸晶体配成100.00mL水溶液;
②用移液管取25.00mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为cmol·L-1KMnO4滴定。滴定时,所发生的反应化学方程式为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
请回答下列问题:
(1)实验①中为配制准确物质的量浓度的草酸溶液,所需用到的仪器是:天平(含砝码)、烧杯、药匙、玻璃棒和
(2)实验②中,滴定时,KMnO4溶液应装在
(3)滴定中,双眼应注视
(4)若滴定是准确的,反应前后的两次读数分别为a和b,则实验测得所配草酸溶液的物质的量浓度为
(5)下列操作,会导致草酸的物质的量浓度偏高的是
| A.滴定前读数准确,终点读数时俯视 |
| B.锥形瓶用蒸馏水洗净后没有用待测液润洗 |
| C.酸式滴定管用蒸馏水洗净后没有用标准液润洗 |
| D.滴定过程中振荡锥形瓶时液滴飞溅出来 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网