单选题 适中0.65 引用1 组卷162
某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g) ΔH<0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g) ΔH<0。图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
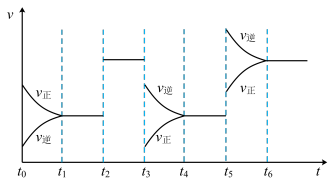
| A.t2时加入了催化剂 | B.t3时降低了温度 |
| C.t5时增大了压强 | D.t3~t4时间内转化率最低 |
21-22高二上·内蒙古赤峰·期中
类题推荐
T ℃时,将6 mol CO2和8 mol H2充入2 L密闭恒容容器中,发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是


| A.反应开始至a点时v(H2)=2 mol/(L·min) |
| B.若曲线Ⅰ对应的条件改变是升温,则该反应放热反应 |
| C.曲线Ⅱ对应的条件改变是降低压强 |
| D.曲线Ⅱ对应的条件改变是加入催化剂 |
在5 L的密闭容器中,一定条件下发生化学反应:2NO(g)+2CO(g) N2(g)+2CO2(g)。起始反应时NO和CO各为3,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
N2(g)+2CO2(g)。起始反应时NO和CO各为3,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
 N2(g)+2CO2(g)。起始反应时NO和CO各为3,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是
N2(g)+2CO2(g)。起始反应时NO和CO各为3,保持密闭容器体积不变,10秒钟达到化学平衡,测得N2为1 mol。下列有关反应速率的说法中,正确的是| A.达到平衡后,若将容器体积压缩为2 L,则正反应速率将增大,逆反应速率将减小 |
| B.反应前5秒钟内,用CO表示的平均反应速率为0.04 mol·L-1·s-1 |
| C.当v正(CO)=2v逆(N2)时,该反应中NO的物质的量不再改变 |
| D.保持压强不变,往容器中充入1 mol He,正、逆反应速率都不改变 |
汽车尾气中NO产生的反应为N2(g)+O2(g) 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是
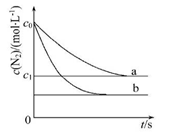
 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是
A.温度T下,该反应的平衡常数K=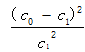 |
| B.若曲线b对应的条件改变是温度,可判断该反应的ΔH<0 |
| C.曲线b对应的条件改变可能是加入了催化剂 |
| D.温度T下,随着反应的进行,混合气体的密度不变 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


