解答题-实验探究题 适中0.65 引用1 组卷117
酸碱中和滴定是一种重要的实验方法,用0.1000mol∙L-1NaOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C.用待测定的溶液润洗酸式滴定管
D.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
E.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至刻度“0”或“0”刻度以下,
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作2~3次
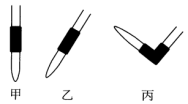
(1)排除碱式滴定管中气泡的方法应采用如图所示操作中的_______ ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
(2)判断滴定终点的现象是:_______ 。
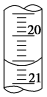
(3)如图是第一次滴定时的滴定管中的液面,其读数为X=_______ mL。
(4)根据下列数据:请计算待测盐酸溶液的浓度:_______ mol/L。(保留四位有效数字)。
(5)在上述实验过程中,出现了以下错误操作(其他操作正确),其中会造成测定结果(待测液浓度值)偏高的有_______ 。
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(6)有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在10mL刻度处,现把管内液体全部流下排出,用量筒接收,得到溶液的体积是_______。
A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C.用待测定的溶液润洗酸式滴定管
D.用酸式滴定管取稀盐酸20.00mL,注入锥形瓶中,加入酚酞
E.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3cm处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至刻度“0”或“0”刻度以下,
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作2~3次
(1)排除碱式滴定管中气泡的方法应采用如图所示操作中的

(2)判断滴定终点的现象是:
(3)如图是第一次滴定时的滴定管中的液面,其读数为X=

(4)根据下列数据:请计算待测盐酸溶液的浓度:
| 滴定次数 | 待测体积 (mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.60 | X |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
A.量取标准液的碱式滴定管未润洗
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(6)有一支50mL的酸式滴定管,其中盛有溶液,液面恰好在10mL刻度处,现把管内液体全部流下排出,用量筒接收,得到溶液的体积是_______。
| A.不能确定 | B.为40mL | C.为10mL | D.大于40mL |
21-22高二上·黑龙江伊春·期末
类题推荐
一个偶然的机会,葛葛和皓皓在实验室发现了一瓶未知浓度的盐酸溶液,作为新时代的好学生,他们欢快地决定用所学知识测定该瓶盐酸的浓度。他们用0.100 0 mol·L-1NaOH溶液滴定该瓶未知浓度的盐酸溶液,其操作可分解为如下几步:
A.用蒸馏水洗干净滴定管
B.检查滴定管是否漏水
C.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
D.另取锥形瓶,再重复操作2~3次
E.用待测定的溶液润洗酸式滴定管
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
G.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞
完成以下填空:
(1)正确操作的顺序是________ 。
(2)判断滴定终点的现象是:锥形瓶中溶液从________ 色变为________ 色,且半分钟内不变色。
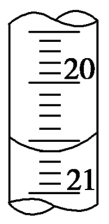
(3)如图是葛葛和皓皓第一次滴定时的滴定管中的液面,其读数为X=________ mL。
(4)根据下列数据:请计算待测盐酸溶液的浓度:________ mol/L。
(5)在上述实验过程中,他们的好朋友发现他们出现了以下错误操作(其他操作正确),其中会造成测定结果(待测液浓度值)偏高的有________ 。
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(6)常温下,他们用0.100 0 mol·L-1NaOH溶液分别滴定20.00 mL 0.200 0 mol·L-1HCl溶液和20.00 mL 0.200 0 mol·L-1CH3COOH溶液,得到2条滴定曲线,如图所示。
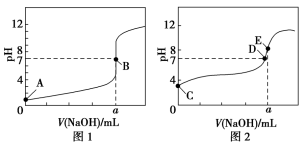
滴定醋酸溶液的曲线是________ (填“图1”或“图2”);滴定曲线中a=________ mL。
A.用蒸馏水洗干净滴定管
B.检查滴定管是否漏水
C.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
D.另取锥形瓶,再重复操作2~3次
E.用待测定的溶液润洗酸式滴定管
F.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下
G.用酸式滴定管取稀盐酸20.00 mL,注入锥形瓶中,加入酚酞
完成以下填空:
(1)正确操作的顺序是
(2)判断滴定终点的现象是:锥形瓶中溶液从
(3)如图是葛葛和皓皓第一次滴定时的滴定管中的液面,其读数为X=

(4)根据下列数据:请计算待测盐酸溶液的浓度:
| 滴定次数 | 待测体积 (mL) | 标准烧碱体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.60 | X |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用待测稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(6)常温下,他们用0.100 0 mol·L-1NaOH溶液分别滴定20.00 mL 0.200 0 mol·L-1HCl溶液和20.00 mL 0.200 0 mol·L-1CH3COOH溶液,得到2条滴定曲线,如图所示。

滴定醋酸溶液的曲线是
酸碱中和滴定是一种重要的实验方法,用 溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C._______
D.用酸式滴定管取稀盐酸 ,移入锥形瓶中,加入酚酞溶液
,移入锥形瓶中,加入酚酞溶液
E.取下碱式滴定管,用标准 溶液润洗后,将标准液注入碱式滴定管“0”刻度以上
溶液润洗后,将标准液注入碱式滴定管“0”刻度以上 处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至“0”刻度或“0”刻度以下,记下滴定管液面所在刻度
处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至“0”刻度或“0”刻度以下,记下滴定管液面所在刻度
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作2~3次
完成以下填空:
(1)C操作为_______
(2)如图是第一次滴定时的滴定管中的液面,其读数为
_______ .
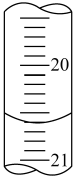
(3)根据下表数据计算待测盐酸的浓度:_______  .
.
(4)在上述实验过程中,出现了以下操作(其他操作均正确),其中会造成测定结果(待测液浓度值)偏高的有_______ (填标号).
A.锥形瓶水洗后直接装待测液
B.碱式滴定管水洗后未用标准 溶液液润洗
溶液液润洗
C.滴定到达终点时,俯视液面读数
D.滴定结束后,碱式滴定管尖嘴处挂有半滴标准液
E.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(5)利用反应 可以定量测定市售硫代硫酸钠(
可以定量测定市售硫代硫酸钠( )的纯度,现在称取
)的纯度,现在称取 硫代硫酸钠固体样品,配成
硫代硫酸钠固体样品,配成 溶液,取
溶液,取 置于锥形瓶中,加入几滴淀粉溶液做指示剂,用含碘
置于锥形瓶中,加入几滴淀粉溶液做指示剂,用含碘 的碘水滴定,消耗碘水
的碘水滴定,消耗碘水 ,则:
,则:
①判定滴定终点的现象为_______
②样品中硫代硫酸钠纯度为_______
A.检查滴定管是否漏水
B.用蒸馏水洗干净滴定管
C._______
D.用酸式滴定管取稀盐酸
E.取下碱式滴定管,用标准
F.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
G.另取锥形瓶,再重复操作2~3次
完成以下填空:
(1)C操作为
(2)如图是第一次滴定时的滴定管中的液面,其读数为

(3)根据下表数据计算待测盐酸的浓度:
| 滴定次数 | 待测盐酸体积( | 标准 | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.60 | X |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
A.锥形瓶水洗后直接装待测液
B.碱式滴定管水洗后未用标准
C.滴定到达终点时,俯视液面读数
D.滴定结束后,碱式滴定管尖嘴处挂有半滴标准液
E.滴定前碱式滴定管尖嘴部分有气泡,滴定后消失
(5)利用反应
①判定滴定终点的现象为
②样品中硫代硫酸钠纯度为
酸碱中和滴定是一种重要的实验方法,用 溶液滴定未知浓度的盐酸,其操作可分为如下几步:①_______ ②用蒸馏水洗干净滴定管 ③_______ ④用酸式滴定管取稀盐酸
溶液滴定未知浓度的盐酸,其操作可分为如下几步:①_______ ②用蒸馏水洗干净滴定管 ③_______ ④用酸式滴定管取稀盐酸 ,注入锥形瓶中,并加入2滴酚酞溶液⑤取下碱式滴定管,用标准
,注入锥形瓶中,并加入2滴酚酞溶液⑤取下碱式滴定管,用标准 溶液润洗后,将标准液注入碱式滴定管“0”刻度以上
溶液润洗后,将标准液注入碱式滴定管“0”刻度以上 处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至“0”刻度或“0”刻度以下,记下滴定管液面所在刻度⑥把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度⑦另取锥形瓶,再重复操作2~3次。完成以下填空:
处,再把碱式滴定管固定好,并排出尖嘴部分的气泡,调节液面至“0”刻度或“0”刻度以下,记下滴定管液面所在刻度⑥把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度⑦另取锥形瓶,再重复操作2~3次。完成以下填空:
(1)填写以上步骤①和③的内容:步骤①_______ ;步骤③_______
(2)如图是第一次滴定时的滴定管中的液面,其读数为 ,
,
_______ 。

(3)根据下表数据计算待测盐酸的浓度:_______  。
。
(4)判断滴定终点的现象为:滴入最后一滴溶液时,_______ 。
(5)在上述实验过程中,出现了以下操作(其他操作均正确),其中会造成测定结果(待测液浓度值)偏高的有_______(填选项字母)。
(6)滴定前装有标准液的滴定管排气泡时,应选择图中的_______(填选项)。
(1)填写以上步骤①和③的内容:步骤①
(2)如图是第一次滴定时的滴定管中的液面,其读数为

(3)根据下表数据计算待测盐酸的浓度:
| 滴定次数 | 待测盐酸体积( | 标准 | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 16.00 | 0.60 | X |
| 第二次 | 16.00 | 2.00 | 24.10 |
| 第三次 | 16.00 | 4.00 | 24.01 |
| 第四次 | 16.00 | 0.90 | 20.89 |
(4)判断滴定终点的现象为:滴入最后一滴溶液时,
(5)在上述实验过程中,出现了以下操作(其他操作均正确),其中会造成测定结果(待测液浓度值)偏高的有_______(填选项字母)。
| A.量取标准液的碱式滴定管未润洗 | B.锥形瓶水洗后直接装待测液 |
| C.滴定完成后碱式滴定管尖嘴部分有气泡 | D.滴定到达终点时仰视液面读数 |
(6)滴定前装有标准液的滴定管排气泡时,应选择图中的_______(填选项)。
A. | B. | C. | D. |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


