解答题-原理综合题 适中0.65 引用1 组卷54
回答下列问题
(1)二甲醚又称甲醚,简称DME,结构简式为CH3OCH3,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。
CO(g)+2H2(g)=CH3OH(g) ΔH1=−90.1kJ⋅mol−1
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2=−49.0kJ⋅mol−1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=−41.1kJ⋅mol−1
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH4=−24.5kJ⋅mol−1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为_______ ;
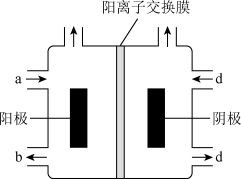
(2)二甲醚还可作燃料电池的燃料,以H2SO4作为电解质,一极充入二甲醚,另一极充入空气和CO2气体。
①该电池的负极反应式为_______ 。
②如图,若b极通入二甲醚,则电解池的阳极反应式为_______ ;若a极通入二甲醚,电解池的反应式为_______ ,当有1mol的二甲醚参与反应时,电解池阳极附近生成的气体的体积(标准状况下)为_______ 。
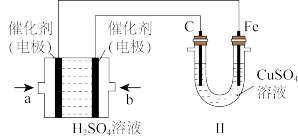
③用该二甲醚燃料电池电解300mL饱和食盐水。电解一段时间后,当溶液pH值为13(室温下测定)时,消耗二甲醚的物质量为_______ 。(忽略溶液体积变化,不考虑损耗)
(1)二甲醚又称甲醚,简称DME,结构简式为CH3OCH3,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。
CO(g)+2H2(g)=CH3OH(g) ΔH1=−90.1kJ⋅mol−1
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2=−49.0kJ⋅mol−1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=−41.1kJ⋅mol−1
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH4=−24.5kJ⋅mol−1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为
(2)二甲醚还可作燃料电池的燃料,以H2SO4作为电解质,一极充入二甲醚,另一极充入空气和CO2气体。
①该电池的负极反应式为
②如图,若b极通入二甲醚,则电解池的阳极反应式为
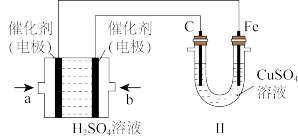
③用该二甲醚燃料电池电解300mL饱和食盐水。电解一段时间后,当溶液pH值为13(室温下测定)时,消耗二甲醚的物质量为
21-22高二·湖北孝感·期末
类题推荐
Ⅰ.二甲醚又称甲醚,简称DME,结构简式为 ,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。
,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。
(1)







由H2和CO直接制备二甲酵(另一产物为水蒸气)的热化学方程式为___________
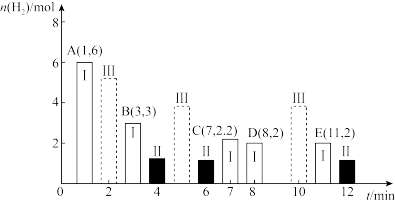
(2)T℃时,在2L密闭容器中充入4molCO和8molH2发生制备二甲醚的反应:
 (没有配平),测得环的物质的量随时间的变化情况如图中状态Ⅰ所示。
(没有配平),测得环的物质的量随时间的变化情况如图中状态Ⅰ所示。
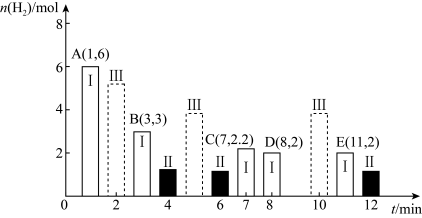
①T℃时,反应的平衡常数K1=___________ 。
②若仅改变某一条件,测得B的物质的最随时间的变化情况如图中状态Ⅱ所示,则K1___________ K2(填“>”、“<”或“=”)。
③若仅改变某一条件,测得B的物质的量随时间的变化情况如图中状态Ⅲ所示,则改变的条件可能是___________ 。
(3)燃料电池是一种绿色环保、高效的化学电源。二甲醚还可作燃料电池的燃料,以熔融 作为电解质,一极充入二甲醚,另一极充入空气和
作为电解质,一极充入二甲醚,另一极充入空气和 气体,该电池的负极反应式为
气体,该电池的负极反应式为___________ 。用该二甲醚燃料电池电解300mL饱和食盐水。电解一段时间后,当溶液的pH值为13(室温下测定)时,消耗二甲醛的质量为___________ g.(忽略溶液体积变化,不考虑损耗)
Ⅱ.25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)25℃时,0.1mol/L的 溶液呈
溶液呈___________ (填“酸性”、“碱性”或“中性”)
(2)用足量 溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为
溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为___________ 。
(3)25℃时,取浓度均为0.1000mol/L的醋酸溶液和氨水溶液各20.00mL,分别用0.1000mol/LNaOH溶液、0.1000mol/L盐酸进行中和滴定,滴定过程中溶液pH随滴加溶液的体积变化关系如图所示。下列说法错误的是_____________
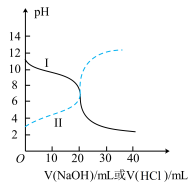
a.曲线Ⅰ,滴加溶液到10mL时:
b.当NaOH溶液和盐酸滴加至20.00mL时,曲线Ⅰ和Ⅱ刚好相交
c.曲线Ⅱ:滴加溶液到10.00mL时,溶液中
d.在逐滴加入NaOH溶液或盐酸至40.00mL的过程中,水的电离程度先增大后减小
(1)
由H2和CO直接制备二甲酵(另一产物为水蒸气)的热化学方程式为
(2)T℃时,在2L密闭容器中充入4molCO和8molH2发生制备二甲醚的反应:

①T℃时,反应的平衡常数K1=
②若仅改变某一条件,测得B的物质的最随时间的变化情况如图中状态Ⅱ所示,则K1
③若仅改变某一条件,测得B的物质的量随时间的变化情况如图中状态Ⅲ所示,则改变的条件可能是
(3)燃料电池是一种绿色环保、高效的化学电源。二甲醚还可作燃料电池的燃料,以熔融
Ⅱ.25℃时,部分物质的电离平衡常数如表所示:
| 化学式 | |||||
| 电离平衡常数 |
(1)25℃时,0.1mol/L的
(2)用足量
(3)25℃时,取浓度均为0.1000mol/L的醋酸溶液和氨水溶液各20.00mL,分别用0.1000mol/LNaOH溶液、0.1000mol/L盐酸进行中和滴定,滴定过程中溶液pH随滴加溶液的体积变化关系如图所示。下列说法错误的是

a.曲线Ⅰ,滴加溶液到10mL时:
b.当NaOH溶液和盐酸滴加至20.00mL时,曲线Ⅰ和Ⅱ刚好相交
c.曲线Ⅱ:滴加溶液到10.00mL时,溶液中
d.在逐滴加入NaOH溶液或盐酸至40.00mL的过程中,水的电离程度先增大后减小
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网