多选题 适中0.65 引用3 组卷235
粗铜中一般含有锌、铁、银、金等杂质。在如图所示的装置中,甲池的总反应方程式为2CH3OH+3O2+4KOH=2K2CO3+6H2O。接通电路一段时间后,精Cu电极质量增加了3.2 g。在此过程中,下列说法正确的是
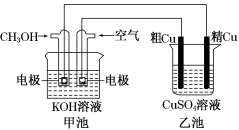
| A.乙池中CuSO4溶液的浓度减小 |
| B.甲池中理论上消耗标准状况下空气的体积是2.8 L(空气中O2体积分数以20%计算) |
| C.甲池是电能转化为化学能的装置,乙池是化学能转化为电能的装置 |
| D.甲池通入CH3OH一极的电极反应为CH3OH-6e-+2H2O=CO |
21-22高二上·山东济南·阶段练习
类题推荐
如下图所示,其中甲池的总反应式为:2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列说法正确的是
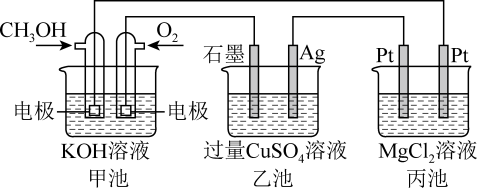

| A.甲池中消耗280 mL(标准状况下)O2,此时丙池中理论上最多产生2.24L的气体 |
| B.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体,能使CuSO4溶液恢复到原浓度 |
| D.甲池通入CH3OH的电极反应为CH3OH-6e-+8OH-=CO |
如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是
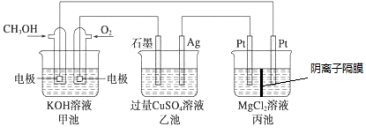

| A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| B.甲池通入CH3OH的电极反应式为CH3OH-6e-+2H2O=CO32-+8H+ |
| C.反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使溶液恢复原浓度 |
| D.甲池中消耗4.48L(标准状况下)O2,此时丙池中理论上最多产生23.2 g固体 |
如图所示,甲池的总反应式为2CH3OH+3O2+4KOH= =2K2CO3+6H2O。下列说法正确的是
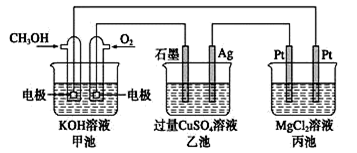

| A.甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 |
| B.甲池通入CH3OH的电极反应为CH3OH- 6e-+ 2H2O= |
| C.甲池中消耗560 mL(标准状况下) O2,此时乙池中银极增重3.2g |
| D.反应一段时间后,向丙池中加入一定量盐酸,一定能使MgCl2溶液恢复到原浓度 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


