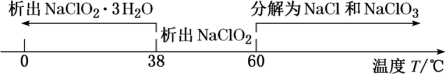解答题-实验探究题 适中0.65 引用3 组卷258
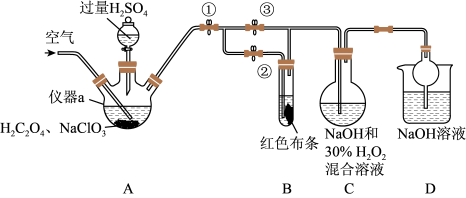
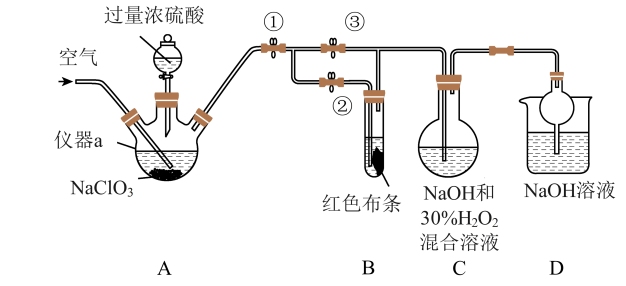
ClO2又称百毒净,可用于水的消毒和纸张、纺织品的漂白。用如图所示装置(夹持装置和加热装置省略)制备ClO2,并探究ClO2的某些性质。
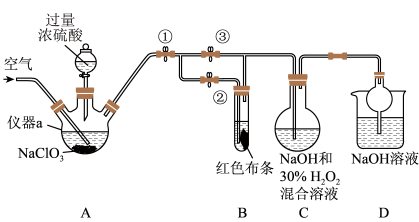
已知:①浓硫酸能与硫酸钠反应,产物为硫酸氢钠。
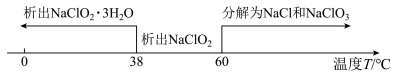
②饱和NaClO2溶液随温度变化情况如下:
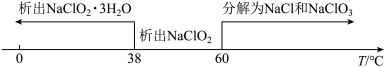
回答下列问题:
(1)写出装置A制备ClO2,同时生成高氯酸(HClO4)的化学方程式:_______ 。
(2)关闭止水夹②,打开止水夹①③,通入一段时间空气,装置C中生成NaClO2,离子方程式为_______ 。若关闭止水夹③,打开止水夹②,B中可观察到的现象为_______ 。
(3)从装置C反应后的溶液中获得NaClO2晶体,需控温在_______ 范围内进行减压蒸发结晶,采用减压蒸发的原因是_______ 。
(4)下列说法不正确的是_______(填字母)。
(5)城市饮用水处理新技术用NaClO2、高铁酸钠替代Cl2。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的顺序是_______ 。

已知:①浓硫酸能与硫酸钠反应,产物为硫酸氢钠。
②饱和NaClO2溶液随温度变化情况如下:

回答下列问题:
(1)写出装置A制备ClO2,同时生成高氯酸(HClO4)的化学方程式:
(2)关闭止水夹②,打开止水夹①③,通入一段时间空气,装置C中生成NaClO2,离子方程式为
(3)从装置C反应后的溶液中获得NaClO2晶体,需控温在
(4)下列说法不正确的是_______(填字母)。
| A.通入的空气可将A中产生的ClO2全部驱赶到C中 |
| B.ClO2处理饮用水时残留的 |
| C.工业上将ClO2气体制成NaClO2固体,其主要目的是便于贮存和运输 |
| D.用Cl2和NaClO2制备ClO2,氧化剂与还原剂物质的量之比为2:1 |
21-22高一下·福建莆田·开学考试
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网