解答题-原理综合题 适中0.65 引用2 组卷125
回答下列问题:
(1)①25℃时,三种弱电解质的电离平衡常数如表:
下列方法中,可以使 溶液中
溶液中 电离程度增大的是
电离程度增大的是_______ 。
a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
(2)常温下, 的
的 溶液加水稀释过程,下列表达式的数据一定变小的是
溶液加水稀释过程,下列表达式的数据一定变小的是_______ 。
a. b.
b. c.
c. d.
d.
(3)常温下,有pH相同、体积相同的a. 溶液和b.HCl溶液,现采取以下措施:
溶液和b.HCl溶液,现采取以下措施:
①分别加适量醋酸钠晶体后, 溶液中
溶液中
_______ HCl溶液中 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
②分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积: 溶液
溶液_______ (填“>”“<”或“=”)HCl溶液。
③温度都升高20℃, 溶液中
溶液中
_______ (填“>”“<”或“=”)HCl溶液中 。
。
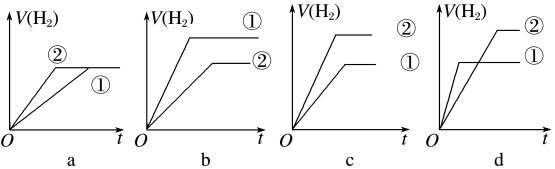
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)
a. b.
b. 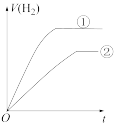 c.
c.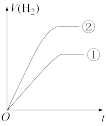 d.
d.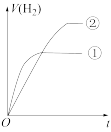
(4)常温下,等体积等物质的量浓度的 和
和 溶液混合后,溶液的
溶液混合后,溶液的
_______ ,等物质的量浓度的① ②
② ③
③ ④
④ 溶液的pH大小顺序是
溶液的pH大小顺序是_______ (填序号); 溶液滴入
溶液滴入 中的离子方程式
中的离子方程式_______ 。
(1)①25℃时,三种弱电解质的电离平衡常数如表:
| 化学式 | HCOOH | |||
| 电离平衡常数 |
a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
(2)常温下,
a.
(3)常温下,有pH相同、体积相同的a.
①分别加适量醋酸钠晶体后,
②分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:
③温度都升高20℃,
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
a.
 b.
b.  c.
c. d.
d.
(4)常温下,等体积等物质的量浓度的
22-23高二上·广东广州·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网