填空题 较易0.85 引用1 组卷81
高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,它的氧化性比高锰酸钾、次氯酸等还强。可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
(1)高铁酸钠中,铁元素的化合价是___________ ;上述制取铁酸钠的反应中,铁元素被___________ (填“还原”或“氧化”)。
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体,使水中悬浮物沉聚。某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
①若将FeCl3溶液分别滴入下列物质中,能形成胶体的是___________ (填序号)。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
②制备方法:将饱和FeCL溶液滴入沸水中,继续煮沸至液体变为___________ 色,停止加热,可得到 Fe(OH)3胶体,发生反应的化学方程式是___________ 。
③Fe(OH)3胶体区别于FeCl3溶液最本质的特征是___________ (填序号)。
A.Fe(OH)3胶体粒子的直径在1~100nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
④下列各项与胶体性质无关的有___________ 。(填序号)
a.卤水点豆腐 b.明矾净水 c.油水分离 d.血液透析
e.酸碱中和 f.三角洲形成 g.制备氢氧化铁沉淀 h。臭氧消毒
(1)高铁酸钠中,铁元素的化合价是
(2)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂原因铁元素转化为Fe(OH)3胶体,使水中悬浮物沉聚。某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
①若将FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
②制备方法:将饱和FeCL溶液滴入沸水中,继续煮沸至液体变为
③Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
A.Fe(OH)3胶体粒子的直径在1~100nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
④下列各项与胶体性质无关的有
a.卤水点豆腐 b.明矾净水 c.油水分离 d.血液透析
e.酸碱中和 f.三角洲形成 g.制备氢氧化铁沉淀 h。臭氧消毒
21-22高一上·云南曲靖·期中
类题推荐
某课外活动小组进行 胶体的制备实验并检验其性质。
胶体的制备实验并检验其性质。
(1)胶体是一种重要的分散系。制备 胶体是向煮沸的蒸馏水中逐滴加入
胶体是向煮沸的蒸馏水中逐滴加入________ (填入“NaOH溶液”或“饱和FeCl3溶液”)溶液,继续煮沸至液体呈________ 色,停止加热。
(2)区分胶体和溶液常用的方法叫________ 。
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________。
(4)高铁酸钠( )是一种新型绿色消毒剂:
)是一种新型绿色消毒剂: 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 胶体,
胶体, 胶体具有吸附性。
胶体具有吸附性。 在处理饮用水的过程中发生了
在处理饮用水的过程中发生了________ (填“氧化还原”或“非氧化还原”)反应。 中铁元素价态为
中铁元素价态为________ 。利用 胶体的吸附性净水,该过程为
胶体的吸附性净水,该过程为________ (填“物理”或“化学”)变化。
(1)胶体是一种重要的分散系。制备
(2)区分胶体和溶液常用的方法叫
(3)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________。
| A. |
| B. |
| C. |
| D. |
回答下列问题:
(1)氧化还原反应与四种基本类型反应的关系如图,则下列化学反应属于区域3的反应是 (填序号)。

(2)高锰酸钾和氢溴酸溶液可以发生如下反应;2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O。
①其中____________ 元素被氧化(填化学式,下同),_________ 作氧化剂。
②在参加反应的HBr中,起还原剂(被氧化)作用的HBr与起酸性作用的HBr的质量之比为____________ 。
(3)某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
①若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是____________ 。
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
②写出制备 Fe(OH)3胶体的化学反应方程式:____________ 。
③Fe(OH)3胶体区别于FeCl3溶液最本质的特征是____________ 。
A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
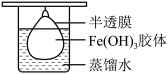
④将制得的胶体放入半透膜制成的袋内,如图所示,放置2 min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察____________ (填“有”或“无”)丁达尔现象。
(1)氧化还原反应与四种基本类型反应的关系如图,则下列化学反应属于区域3的反应是 (填序号)。

| A. |
| B. |
| C. |
| D.Zn+H2SO4=ZnSO4+H2↑ |
①其中
②在参加反应的HBr中,起还原剂(被氧化)作用的HBr与起酸性作用的HBr的质量之比为
(3)某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
①若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是
A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液
②写出制备 Fe(OH)3胶体的化学反应方程式:
③Fe(OH)3胶体区别于FeCl3溶液最本质的特征是
A.Fe(OH)3胶体粒子的直径在1~100 nm之间 B.Fe(OH)3胶体具有丁达尔效应
C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸
④将制得的胶体放入半透膜制成的袋内,如图所示,放置2 min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察

某课外活动小组进行Fe(OH)3胶体的制备实验并检验其性质。
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是___________。
(2)现有甲、乙、丙三名同学进行Fe(OH)3胶体的制备实验正确的是___________ (填序号)。
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
③丙同学向饱和FeCl3溶液中,加入过量的NaOH溶液。
(3)Fe(OH)3胶体制备的化学方程式为___________ 。
(4)证明有Fe(OH)3胶体生成的实验操作是___________ 。利用的胶体性质是___________ 。
(5)Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是___________ (填序号)。
A.胶粒直径大小不同B.颜色不同C.后者不稳定
(6)若向制得的胶体中再加入稀盐酸,红褐色分散系会被破坏,变为黄色溶液,写出相关反应方程式:___________
(1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是___________。
| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
①甲同学的操作是:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至混合液呈红褐色,停止加热。
②乙同学向沸水中滴加饱和FeCl3溶液,为了使反应进行充分,煮沸10分钟。
③丙同学向饱和FeCl3溶液中,加入过量的NaOH溶液。
(3)Fe(OH)3胶体制备的化学方程式为
(4)证明有Fe(OH)3胶体生成的实验操作是
(5)Fe(OH)3胶体与Fe(OH)3沉淀的本质区别是
A.胶粒直径大小不同B.颜色不同C.后者不稳定
(6)若向制得的胶体中再加入稀盐酸,红褐色分散系会被破坏,变为黄色溶液,写出相关反应方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


