单选题 适中0.65 引用5 组卷734
利用 和
和 合成甲醇,可以减少
合成甲醇,可以减少 的排放,实现碳的循环利用。涉及的主要反应如下:
的排放,实现碳的循环利用。涉及的主要反应如下:
反应Ⅰ:
反应Ⅱ:
在 密闭容器中通入
密闭容器中通入 和
和 ,选择合适的催化剂反应,甲醇的选择率(生成甲醇的
,选择合适的催化剂反应,甲醇的选择率(生成甲醇的 占
占 总转化量的物质的量分数)和
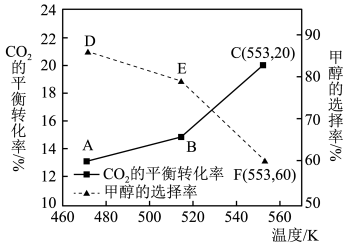
总转化量的物质的量分数)和 的平衡转化率随温度的变化趋势如图所示。下列说法正确的是
的平衡转化率随温度的变化趋势如图所示。下列说法正确的是
反应Ⅰ:
反应Ⅱ:
在

| A. |
| B. |
| C.高温下使用更高效的催化剂提高甲醇的平衡产率 |
| D.其它条件不变,增大压强可提高平衡时 |
22-23高三上·江苏南京·阶段练习
类题推荐
二氧化碳加氢制甲醇可以实现温室气体资源化利用,过程中的主要反应为



密闭容器中,反应物起始物质的量比 时,在不同条件下(①温度为250℃下压强变化,②压强为
时,在不同条件下(①温度为250℃下压强变化,②压强为 下温度变化)达到平衡时
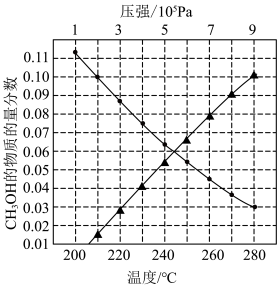
下温度变化)达到平衡时 物质的量分数变化如图所示。下列有关说法正确的是
物质的量分数变化如图所示。下列有关说法正确的是
密闭容器中,反应物起始物质的量比
| A.反应 |
| B.在250℃、 |
| C.当甲醇的物质的量分数为0.03时, |
| D.提高 |
CO2的资源化利用能有效减少CO2排放缓解能源危机。用CO2、H2为原料合成甲醇(CH3OH)过程主要涉及以下反应:
a)

b)

c)

(1)根据盖斯定律,反应a的 =
=_______ 。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
(3)加压,甲醇产率将_______ ;若原料二氧化碳中掺混一氧化碳,随一氧化碳含量的增加,甲醇产率将_______ 。(填“升高”、“不变”、“降低”或“无法确定”)。
(4)使用新型催化剂,让1molCO2和3molH2在1L密闭容器中只发生反应a、b,CO2平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的CO2物质的量分数)随温度的变化趋势如图所示。

553K时,若反应后体系的总压为p,反应a的
_______ (列出计算式即可)。( 为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数)由上图可知,适宜的反应温度为
为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数)由上图可知,适宜的反应温度为_______ K。
a)
b)
c)
(1)根据盖斯定律,反应a的
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
| A.升高温度,反应b正向移动,反应c逆向移动 |
| B.加入反应a的催化剂,可以降低反应的活化能及反应热 |
| C.增大H2的浓度,有利于提高CO2的平衡转化率 |
| D.及时分离除CH3OH,可以使得反应a的正反应速率增大 |
(4)使用新型催化剂,让1molCO2和3molH2在1L密闭容器中只发生反应a、b,CO2平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的CO2物质的量分数)随温度的变化趋势如图所示。

553K时,若反应后体系的总压为p,反应a的
二氧化碳催化加氢制甲醇是一种实现“碳中和”的有效方法。该过程通过如下步骤实现:
①CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41kJ·mol-1
CO(g)+H2O(g) ΔH=+41kJ·mol-1
②CO(g)+2H2(g) CH3OH(g) ΔH=-90kJ·mol-1
CH3OH(g) ΔH=-90kJ·mol-1
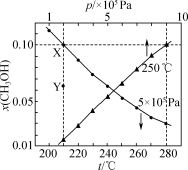
在密闭容器中,反应物起始物质的量比 =3,一定条件下达到平衡时,甲醇的物质的量分数x(CH3OH)随压强或温度变化的曲线如图所示。下列说法正确的是
=3,一定条件下达到平衡时,甲醇的物质的量分数x(CH3OH)随压强或温度变化的曲线如图所示。下列说法正确的是
①CO2(g)+H2(g)
②CO(g)+2H2(g)
在密闭容器中,反应物起始物质的量比
| A.二氧化碳加氢制甲醇的总反应可表示为CO2(g)+3H2(g) |
| B.在210℃,5×105Pa下,反应至x(CH3OH)达到Y点的值时,延长反应时间不能使x(CH3OH)达到X点 |
| C.保持其他条件不变,增大起始物 |
| D.为高效利用CO2,需研发低温下CO2转化率高和甲醇选择性高的催化剂 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


