解答题-原理综合题 适中0.65 引用1 组卷134
回答下列问题:
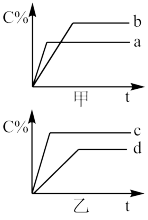
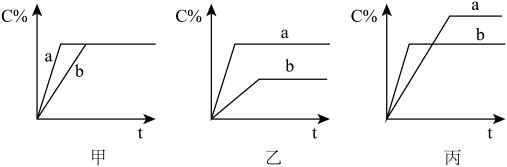
(1)现有可逆反应A(气)+B(气) 3C(气),图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
3C(气),图中甲、乙、丙分别表示在不同的条件下,生成物C在反应混和物中的百分含量(C%)和反应时间的关系:
①若乙图中的a曲线表示200℃时的情况,b曲线表示100℃时的情况,则此可逆反应的正反应是____ 热反应。
②若丙图中两条曲线分别表示不同压强下的情况,则____ 曲线是表示压强较大的情况。
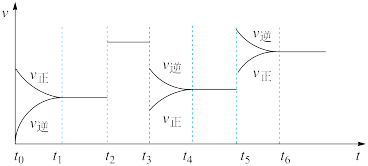
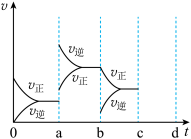
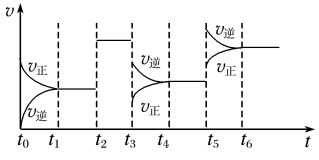
(2)图中Z表示在密闭容器中反应:2SO2+O2 2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,t3至t4过程中改变的条件可能是
2SO3 ΔH<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,t3至t4过程中改变的条件可能是____ ;t5至t6过程中改变的条件可能是____ ;写出t1至t2阶段平衡体系中反应平衡常数的表达式K=____ 。
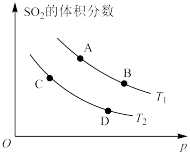
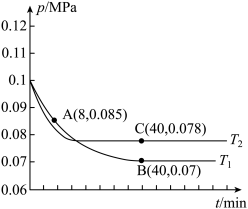
(3)如图表示平衡时SO2的体积分数随压强和温度变化的曲线,则:
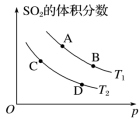
①温度关系:T1____ T2(填“>”“<”或“=”,下同)。
②平衡常数关系:K(A)____ K(D)。
(1)现有可逆反应A(气)+B(气)

①若乙图中的a曲线表示200℃时的情况,b曲线表示100℃时的情况,则此可逆反应的正反应是
②若丙图中两条曲线分别表示不同压强下的情况,则
(2)图中Z表示在密闭容器中反应:2SO2+O2

(3)如图表示平衡时SO2的体积分数随压强和温度变化的曲线,则:

①温度关系:T1
②平衡常数关系:K(A)
21-22高二上·甘肃武威·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网