解答题-实验探究题 适中0.65 引用1 组卷115
某实验探究小组用酸性 KMnO4溶液与H2C2O4溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性 KMnO4溶液的浓度可选择 0.010 mol·L-1、0.001 mol·L-1,催化剂的用量可选择 0.5 g、0 g,实验温度可选择 298K 、323K。每次实验酸性KMnO4溶液的用量均为 4 mL,H2C2O4溶液(0.100 mol·L-1)的用量均为2 mL。
(1)写出反应的离子方程式:_______ 。
(2)请完成实验设计表:
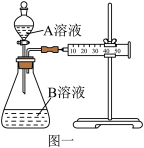
(3)图一通过测定一定时间内 CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
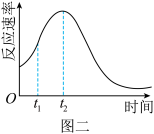
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物 MnSO4是该反应的催化剂;②_______ 。
(1)写出反应的离子方程式:
(2)请完成实验设计表:
| 编号 | T/K | 催化剂的用量/g | 酸性 KMnO4溶液的浓度/(mol·L-1) | 实验目的 |
| ① | 298 | 0.5 | 0.010 | a.实验①和②探究 b.实验①和③探究 c.实验①和④探究催化剂对该反应速率的影响。 |
| ② | 298 | 0.5 | 0.001 | |
| ③ | 323 | 0.5 | 0.010 | |
| ④ | 0 |

(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①产物 MnSO4是该反应的催化剂;②

22-23高二上·广东惠州·期中
类题推荐
某小组利用弱酸H2C2O4溶液和酸性KMnO4溶液(H2SO4酸化)反应来探究“外界条件对化学反应速率的影响”。该小组欲通过测定单位时间内生成CO2的体积来判断反应的快慢。设计实验方案如表:
(1)已知反应后H2C2O4转化为CO2逸出,MnO 转化为Mn2+,写出该反应的离子方程式
转化为Mn2+,写出该反应的离子方程式_____ ;每消耗1molH2C2O4,则反应中转移____ mol电子。
(2)探究浓度对化学反应速率影响的实验编号是____ ,实验②、③探究____ 对化学反应速率影响。本实验还可通过测定____ 来比较化学反应速率。
(3)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

a.该反应放热,使体系温度升高;
b._____ 。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| ① | 0.10 | 20 | 0.10 | 30 | 25 |
| ② | 0.20 | 20 | 0.10 | 30 | 25 |
| ③ | 0.20 | 20 | 0.10 | 30 | 50 |
(2)探究浓度对化学反应速率影响的实验编号是
(3)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

a.该反应放热,使体系温度升高;
b.
某实验探究小组用酸性 溶液与
溶液与 溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性
溶液反应过程中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件如下:所用酸性 溶液的浓度可选择0.010mol/L、0.001mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性
溶液的浓度可选择0.010mol/L、0.001mol/L,催化剂的用量可选择0.5g、0g,实验温度可选择298K、323K。每次实验酸性 溶液的用量均为4mL,
溶液的用量均为4mL, 溶液(0.100mol/L)的用量均为2mL。
溶液(0.100mol/L)的用量均为2mL。
已知 。
。
(1)写出反应的离子方程式:___________ 。
(2)已知部分实验数据如下:
实验目的:
a.实验①和②探究___________ 对该反应速率的影响;
b.实验①和③探究___________ 对该反应速率的影响;
c.实验①和④探究催化剂对该反应速率的影响,则实验④选择温度___________ K,催化剂用量g,酸性 溶液的浓度
溶液的浓度___________ mol/L。该反应的催化剂应选择___________ (填写“ ”或“
”或“ ”)。
”)。
已知
(1)写出反应的离子方程式:
(2)已知部分实验数据如下:
| 实验编号 | T/K | 催化剂的用量/g | 酸性 |
| ① | 298 | 0.5 | 0.010 |
| ② | 298 | 0.5 | 0.001 |
| ③ | 323 | 0.5 | 0.010 |
| ④ |
a.实验①和②探究
b.实验①和③探究
c.实验①和④探究催化剂对该反应速率的影响,则实验④选择温度
某小组利用H2C2O4溶液和酸性KMnO4溶液(H2SO4酸化)反应来探究“外界条件对化学反应速率的影响”。该小组欲通过测定单位时间内生成CO2的体积来判断反应的快慢。设计实验方案如下:
(1)已知反应后H2C2O4转化为CO2逸出, 转化为Mn2+,写出该反应的离子方程式
转化为Mn2+,写出该反应的离子方程式______________ ;每消耗1 molH2C2O4,则反应中转移________________ mol电子。
(2)探究浓度对化学反应速率影响的实验编号是_________ ,实验②、③探究_________ 对化学反应速率影响。本实验还可通过测定____________ 来比较化学反应速率。
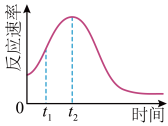
(3)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:a、该反应放热,使体系温度升高;b、____________ 。
(4)若实验①在5 min末收集49.0 mLCO2气体,则在5 min末,c( )=
)=_______ mol•L-1。(已知25℃时,气体摩尔体积Vm=24.5 L• mol-1)
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 20 | 0.10 | 30 | 25 |
| ② | 0.20 | 20 | 0.10 | 30 | 25 |
| ③ | 0.20 | 20 | 0.10 | 30 | 50 |
(2)探究浓度对化学反应速率影响的实验编号是
(3)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:a、该反应放热,使体系温度升高;b、

(4)若实验①在5 min末收集49.0 mLCO2气体,则在5 min末,c(
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


