单选题 适中0.65 引用1 组卷175
硫化氢(H2S)是一种有毒气体,广泛存在于石油化工、冶金等行业的废气中,常用足量纯碱溶液吸收法、热分解法、Fe2(SO4)3溶液氧化脱除法、活性炭吸附氧化法脱除。同时,H2S也是一种重要的化工原料,可以用来制备硫磺、苯硫酚(C6H5SH)、H2S、NaHS还常用于脱除水体中的Cu2+,形成黑色、不溶于稀硫酸的CuS沉淀。室温时,通过下列实验探究NaHS溶液的性质
下列有关说法不正确 的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测量0.1 mol/L NaHS溶液的pH,测得pH约为7.8 |
| 2 | 将浓度均为0.001 mol/L NaHS溶液与CuSO4溶液等体积混合,有黑色沉淀产生 |
| A.0.1 mol/L NaHS溶液中有:c(H2S)>c(S2—) |
| B.0.1 mol/L NaHS溶液中存在:c(H+)+c(H2S)= c(OH—)+2c(S2—) |
| C.实验2发生反应的离子方程式:HS—+ Cu2+ = CuS↓+ H+ |
| D.实验2的上层清液中c(H+)·c(OH—)=1×10—14 |
22-23高二上·江苏南通·期中
类题推荐
硫化氢(H2S)是一种有毒气体,广泛存在于石油化工、冶金等行业的废气中,常用足量纯碱溶液吸收法、热分解法、Fe2(SO4)3溶液氧化脱除法、活性炭吸附氧化法脱除。同时,H2S也是一种重要的化工原料,可以用来制备硫磺、苯硫酚(C6H5SH)、H2S、NaHS还常用于脱除水体中的Cu2+,形成黑色、不溶于稀硫酸的CuS沉淀。H2S可以在高温下与氯苯(C6H5Cl)反应制备苯硫酚(C6H5SH),同时得到副产物苯(C6H6),发生反应的热化学方程式为:
反应I:C6H5Cl(g)+H2S(g) C6H5SH(g)+HCl(g) △H1
C6H5SH(g)+HCl(g) △H1
反应II: C6H5Cl(g)+H2S(g)=C6H6(g)+HCl(g)+ S8(g) △H2= - 45.8 kJ/mol
S8(g) △H2= - 45.8 kJ/mol
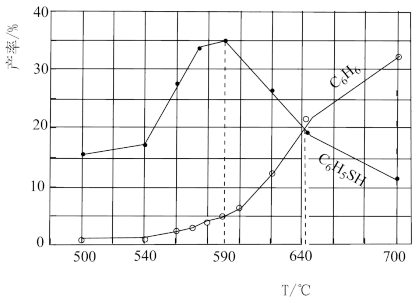
将H2S与C6H5Cl(体积比5:2)加入某恒容密闭容器中,反应20 min后测得混合气中C6H5SH和C6H6的产率(实际产量与理论产量之比)与温度的关系如图所示。下列说法不正确的是
反应I:C6H5Cl(g)+H2S(g)
反应II: C6H5Cl(g)+H2S(g)=C6H6(g)+HCl(g)+
将H2S与C6H5Cl(体积比5:2)加入某恒容密闭容器中,反应20 min后测得混合气中C6H5SH和C6H6的产率(实际产量与理论产量之比)与温度的关系如图所示。下列说法不正确的是

| A.由图可知△H1<0 |
| B.在500℃时,反应II处于平衡状态 |
| C.在590℃时,反应I的平衡常数为 |
| D.在645℃时,延长反应时间,会提高C6H6的产率 |
硫化氢( )是一种有毒气体,水溶液为二元弱酸。烟气中的
)是一种有毒气体,水溶液为二元弱酸。烟气中的 常用
常用 溶液氧化脱除、活性炭吸附氧化脱除。NaHS也常用于脱除水体中的
溶液氧化脱除、活性炭吸附氧化脱除。NaHS也常用于脱除水体中的 ,形成黑色、不溶于稀硫酸的CuS沉淀。室温时,通过下列实验探究NaHS溶液的性质
,形成黑色、不溶于稀硫酸的CuS沉淀。室温时,通过下列实验探究NaHS溶液的性质
下列有关说法不正确 的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测量0.1mol/L NaHS溶液的pH,测得pH约为7.8 |
| 2 | 将浓度均为0.001mo/L NaHS溶液与 |
| A.0.1mol/L NaHS溶液中有: |
| B.0.1mol/L NaHS溶液中有: |
| C.依据实验2的现象,能得出 |
| D.在实验2所得的上层清液中 |
硫化氢(H2S)是一种有毒气体,广泛存在于石油化工、冶金等行业的废气中,常用足量纯碱溶液吸收法、热分解法、Fe2(SO4)3溶液氧化脱除法、活性炭吸附氧化法脱除。同时,H2S也是一种重要的化工原料,可以用来制备硫磺、苯硫酚(C6H5SH)、H2S、NaHS还常用于脱除水体中的Cu2+,形成黑色、不溶于稀硫酸的CuS沉淀。Fe2(SO4)3溶液与表面喷淋水的活性炭分别处理H2S的原理如阳所示,下列说法正确的是
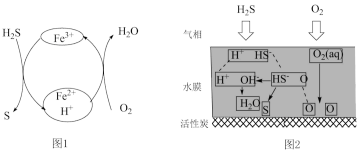

| A.图1中Fe2(SO4)3溶液可循环再生 |
| B.图1脱除34 gH2S,理论上一定消耗11.2 LO2 |
| C.图2中,其他条件不变时,增大水膜的厚度,H2S的氧化去除率增大 |
| D.图2中,其他条件不变时,适当增大水膜的pH,H2S 的氧化去除率下降 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


