解答题-结构与性质 较难0.4 引用1 组卷564
氢能是一种绿色能源,也是重要的还原剂。目前有多种方法可以制氢并储氢。
Ⅰ.NaBH4、氨硼烷(NH3BH3)、MgH2的制氢储氢。
(1)NaBH4与水反应生成H2,可能的反应机理如图-1所示。
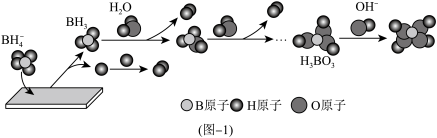
①其他条件不变时,以D2O代替H2O催化释氢,所得气体的分子式为_______ 。
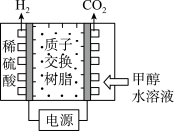
②电解NaBO2溶液可制得NaBH4,电解装置示意图如图-2所示。
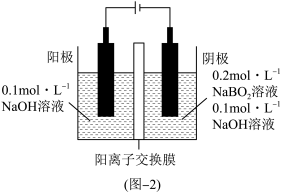
该电解池阴极的电极反应式为_______ 。
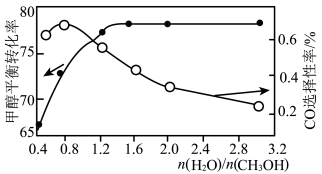
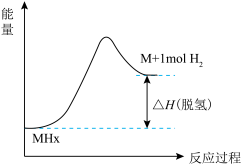
(2)氨硼烷(NH3BH3)可以水解释氢和热分解释氢。受热释氢时固体残留率随温度的变化如图-3所示。
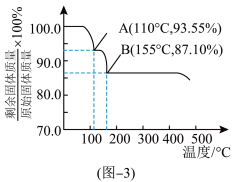
①NH3BH3中B的杂化方式_______ 。
②110℃时NH3BH3分解释氢的化学方程式是_______ 。
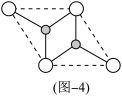
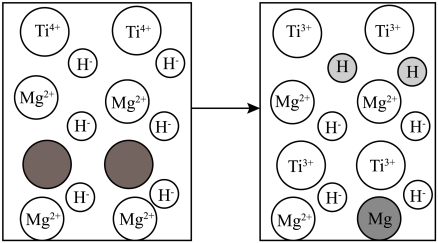
(3)MgH2是一种具有良好的复合储氢材料之一,是一种单层的二维材料,二维晶胞俯视图如图-4,MgH2中,Mg的配位数为_______ 。
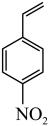
Ⅱ.H2能将4-硝基苯乙烯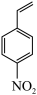 在特定条件下制备4-乙烯基苯胺
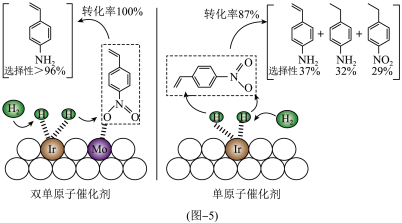
在特定条件下制备4-乙烯基苯胺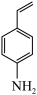 。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图-5所示
。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图-5所示
已知:Mo单原子位点对4-硝基苯乙烯有较好的吸附效果。
(4)①请描述4-硝基苯乙烯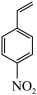 在单原子催化剂下与H2发生反应的过程
在单原子催化剂下与H2发生反应的过程_______ 。
②使用双单原子催化剂,可以大大提高4-乙烯基苯胺的产率,原因是_______ 。
Ⅰ.NaBH4、氨硼烷(NH3BH3)、MgH2的制氢储氢。
(1)NaBH4与水反应生成H2,可能的反应机理如图-1所示。

①其他条件不变时,以D2O代替H2O催化释氢,所得气体的分子式为
②电解NaBO2溶液可制得NaBH4,电解装置示意图如图-2所示。

该电解池阴极的电极反应式为
(2)氨硼烷(NH3BH3)可以水解释氢和热分解释氢。受热释氢时固体残留率随温度的变化如图-3所示。

①NH3BH3中B的杂化方式
②110℃时NH3BH3分解释氢的化学方程式是
(3)MgH2是一种具有良好的复合储氢材料之一,是一种单层的二维材料,二维晶胞俯视图如图-4,MgH2中,Mg的配位数为

Ⅱ.H2能将4-硝基苯乙烯
 在特定条件下制备4-乙烯基苯胺
在特定条件下制备4-乙烯基苯胺 。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图-5所示
。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图-5所示已知:Mo单原子位点对4-硝基苯乙烯有较好的吸附效果。

(4)①请描述4-硝基苯乙烯
 在单原子催化剂下与H2发生反应的过程
在单原子催化剂下与H2发生反应的过程②使用双单原子催化剂,可以大大提高4-乙烯基苯胺的产率,原因是
2022·江苏泰州·模拟预测
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
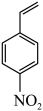 在特定条件下转化为4-乙烯基苯胺
在特定条件下转化为4-乙烯基苯胺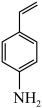 。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图所示。
。两种不同催化剂将4-硝基苯乙烯还原加氢的过程如图所示。
 在单原子催化剂下与
在单原子催化剂下与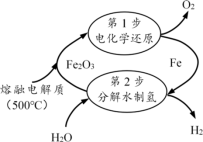
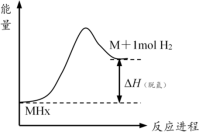

 表示的微粒是
表示的微粒是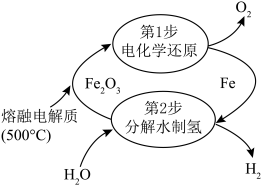
 表示的微粒是
表示的微粒是

