单选题 适中0.65 引用3 组卷195
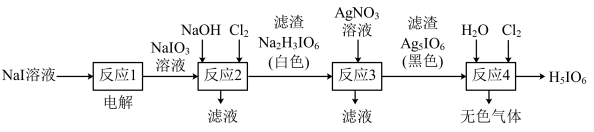
正高碘酸(H5IO6)是白色结晶性粉末,溶于水,主要用作氧化剂和分析试剂。由NaI制取H5IO6的实验流程如图所示:
下列说法正确的是

下列说法正确的是
| A.电解过程中阳极反应为:I-+6OH--6e-=IO |
| B.“反应2”中Cl2与NaIO3的物质的量之比为1∶1 |
| C.“反应3”的滤液中含有NaNO3,NaI等 |
| D.“反应4”为非氧化还原反应 |
22-23高三上·湖北·阶段练习
类题推荐
正高碘酸(H5IO6)是白色结晶性粉末,可溶于水,主要用作氧化剂和分析试剂。由NaI制取H5IO6的实验流程如图所示:
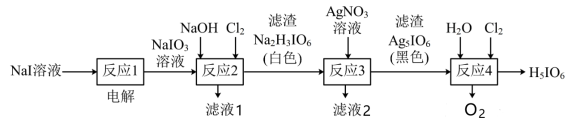
| A.“反应1”中: |
| B.“反应2”中: |
| C.“反应3”中: |
| D.“反应4”中: |
采用水合肼( )还原法制取碘化钠固体,其制备流程如图所示,已知:“合成”步骤中生成的副产物为
)还原法制取碘化钠固体,其制备流程如图所示,已知:“合成”步骤中生成的副产物为 。
。

下列说法中不正确的是

下列说法中不正确的是
| A.“合成”过程所得溶液中主要含有 |
| B.“还原”过程消耗 |
| C.“水合肼还原法”的优点是 |
| D.工业上常用铁屑还原 |
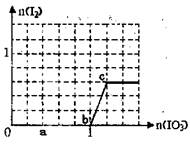
已知:还原性HSO3->I-,氧化性IO3->I2。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液。加入KIO3和析出I2的物质的量的关系曲线如右图所示。下列说法正确的是

| A.反应过程中的氧化产物均为SO3 |
| B.a点时剩余NaHSO3的物质的量为1.2 mol |
| C.b点时的还原产物可能是KI或NaI |
| D.当溶液中I-与I2的物质的量之比为1:1时,加入的KIO3为1.1 mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


