填空题 适中0.65 引用1 组卷33
填空
(1)金属钠与水反应的化学方程式:_______
(2)写出次氯酸见光分解的化学方程式:_______
(3)写出氯气和氢氧化钠溶液反应的离子方程式 :_______
(1)金属钠与水反应的化学方程式:
(2)写出次氯酸见光分解的化学方程式:
(3)写出氯气和氢氧化钠溶液反应的
22-23高一上·浙江嘉兴·阶段练习
类题推荐
I.下图为一个五圆环,每个环中的物质依次为 、NaCl、
、NaCl、 、
、 、
、 ,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
,图中相连的两种物质可归属为同一类,用①、②、③、④表示相交部分,请回答下列问题:
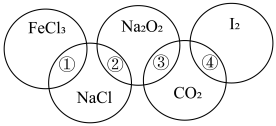
(1)关于上述相交部分的说法不正确 的是___________(填序号)。
(2)上述五种物质中,有两种物质可以发生氧化还原反应,其化学方程式为___________ ;
(3)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1 上图中某物质M的溶液,继续煮沸得到红褐色透明液体。
上图中某物质M的溶液,继续煮沸得到红褐色透明液体。
①物质M的化学式为___________ 。
②检验该红褐色透明液体是胶体的方法为___________ 。
II.写出下列除杂的离子方程式,括号内的物质为杂质。
(4)FeCl2(FeCl3):___________
(5)CO2(HCl):___________
(6)NaHCO3溶液(Na2CO3):___________

(1)关于上述相交部分的说法
| A.①表示盐类 | B.②表示钠的化合物 |
| C.③表示氧化物 | D.④表示非电解质 |
(3)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1
①物质M的化学式为
②检验该红褐色透明液体是胶体的方法为
II.写出下列除杂的离子方程式,括号内的物质为杂质。
(4)FeCl2(FeCl3):
(5)CO2(HCl):
(6)NaHCO3溶液(Na2CO3):
铁的腐蚀和防护与生产、生活密切相关。已知:氢氧化物开始和完全沉淀的pH如下表(开始沉淀时,金属离子的浓度为1.0mol/L)。完成下列问题。
(1)研究铁的腐蚀。将一定量铁粉和碳粉混合后置于一密闭容器中,加入NaCl和盐酸的混合溶液。测得溶液的pH和压强随时间变化的曲线如图所示。

①容器内压强先增大后减小,除温度影响外的原因是___________ 。
②反应过程中,混合液里先生成的Fe2+会被氧化生成Fe(OH)3,反应的离子方程式为___________ 。
③700s后pH略下降,原因是___________ 。
(2)研究铁的防护。在铁表面镀锌可有效防止铁被腐蚀。
已知:溶液中Zn2+与NH3可发生反应:Zn2++nNH3 [ Zn(NH3)n]2+(n= 1~4)。某镀锌废液中含有Zn2+(<1mol/L)、Fe2+、Fe3+、
[ Zn(NH3)n]2+(n= 1~4)。某镀锌废液中含有Zn2+(<1mol/L)、Fe2+、Fe3+、 、H+等阳离子。请设计利用该电镀废液回收ZnCl2-NH4Cl溶液的实验方案:
、H+等阳离子。请设计利用该电镀废液回收ZnCl2-NH4Cl溶液的实验方案:___________ 。(实验中可选用试剂:30%H2O2、1.0mol/LNaOH溶液、1.0mol/L氨水)
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀时的pH | 3.2 | 8.8 | 8.0 |

①容器内压强先增大后减小,除温度影响外的原因是
②反应过程中,混合液里先生成的Fe2+会被氧化生成Fe(OH)3,反应的离子方程式为
③700s后pH略下降,原因是
(2)研究铁的防护。在铁表面镀锌可有效防止铁被腐蚀。
已知:溶液中Zn2+与NH3可发生反应:Zn2++nNH3
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


