解答题-工业流程题 适中0.65 引用2 组卷115
(1)将铬铁矿粉碎的目的是
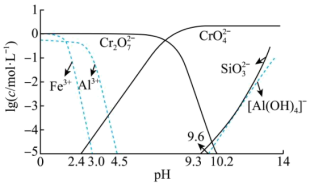
(2)常温下,铬酸
(3)该小组用滴定法准确测得产品中
(4)以
22-23高二上·山西晋城·阶段练习
类题推荐
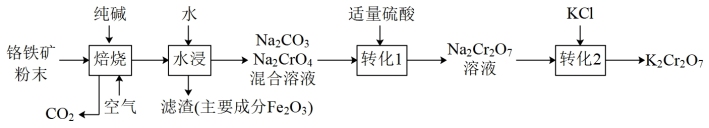
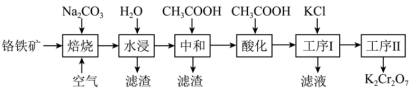
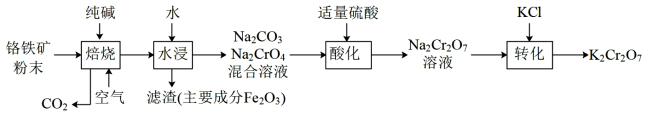
重铬酸钾是一种重要的化工原料,一般由铬铁矿制备。铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:

回答下列问题。
(1)将铬铁矿粉碎有利于加快熔融、氧化的速率,其原理是______________________________ 。
步骤①的主要反应为FeO·Cr2O3 + Na2CO3 +NaNO3 Na2CrO4+ Fe2O3 + CO2+NaNO2(未配平) ,氧化产物为
Na2CrO4+ Fe2O3 + CO2+NaNO2(未配平) ,氧化产物为_________________ ,配平后FeO· Cr2O3与NaNO3的化学计量数之比为______________ 。
(2)下列说法正确的是 。
(3)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩、冷却结晶、过滤得到K2Cr2O7固体。冷却到 (填标号),得到的K2Cr2O7固体产品最多。

(4)某工厂用m1 kg铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到m2 kg K2Cr2O7产率为_______________ (用含m1、m2的代数式表示)。
(5)某小组用分光光度法测定产品纯度(K2Cr2O7溶液的吸光度与其浓度成正比),其中某同学测得的质量分数明显偏低,分析原因,发现配制K2Cr2O7待测溶液时少加了一种试剂。该试剂是________ ,添加该试剂的作用是_______________________________ 。

回答下列问题。
(1)将铬铁矿粉碎有利于加快熔融、氧化的速率,其原理是
步骤①的主要反应为FeO·Cr2O3 + Na2CO3 +NaNO3
(2)下列说法正确的是 。
| A.步骤①可以用陶瓷容器做反应器 |
| B.步骤②低温可提高浸取率 |
| C.步骤③所得滤渣2的主要成分是Al(OH)3 |
| D.步骤④的目的主要是使Na2CrO4转变为Na2Cr2O7 |
(3)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩、冷却结晶、过滤得到K2Cr2O7固体。冷却到 (填标号),得到的K2Cr2O7固体产品最多。

| A.20°C | B.40°C | C.60°C | D.80°C |
(4)某工厂用m1 kg铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到m2 kg K2Cr2O7产率为
(5)某小组用分光光度法测定产品纯度(K2Cr2O7溶液的吸光度与其浓度成正比),其中某同学测得的质量分数明显偏低,分析原因,发现配制K2Cr2O7待测溶液时少加了一种试剂。该试剂是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网