解答题-结构与性质 较易0.85 引用1 组卷113
钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为____ 。Ti在元素周期表中的位置____ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____ 。
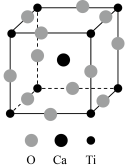
(3)CaTiO3的晶胞如图所示,其组成元素的电负性大小顺序是____ ;金属离子与氧离子间的作用力为____ ,Ca2+的配位数是____ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图所示,其组成元素的电负性大小顺序是

22-23高三上·天津滨海新·期中
类题推荐
钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
(1)基态Ti原子的核外电子排布式为_______ 。
(2)Ti的四卤化物熔点如下表所示:
TiF4熔点高于其他三种卤化物,写出TiF4的电子式_______ ;TiCl4至TiI4熔点依次升高,其原因是_______ 。
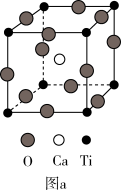
(3)CaTiO3的晶胞如图(a)所示,其组成元素钙位于元素周期表中的_______ 区,晶胞中Ti4+的配位数是_______ 。

(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH ,其晶胞如图(b)所示。有机碱CH3NH
,其晶胞如图(b)所示。有机碱CH3NH 中有配位键,提供空轨道的微粒是
中有配位键,提供空轨道的微粒是_______ ;图(a)中的Ca2+与图(b)中的_______ 空间位置相同。若图(b)中晶胞参数(边长)为anm,则晶体密度为_______ g·cm-3(列出计算式)。

(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示:
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图(a)所示,其组成元素钙位于元素周期表中的

(4)一种立方钙钛矿结构的金属卤化物光电材料的组成为Pb2+、I-和有机碱离子CH3NH

钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为_______ 。
(2)Ti的四卤化物熔点如下表所示:
TiF4熔点高于其他三种卤化物,写出TiF4的电子式_______ ;TiCl4至TiI4熔点依次升高,其原因是_______ 。
(3)CaTiO3的晶胞如图(a)所示,金属离子与氧离子间的作用力为_______ 。
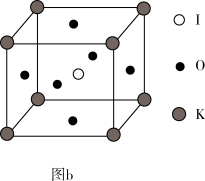
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为anm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图b所示。K与O间的最短距离为_______ nm(用含a的代数式表示),与K紧邻的O个数为_______ 。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则O处于_______ 位置,K处于_______ 位置。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示:
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
TiF4熔点高于其他三种卤化物,写出TiF4的电子式
(3)CaTiO3的晶胞如图(a)所示,金属离子与氧离子间的作用力为

(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为anm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图b所示。K与O间的最短距离为

(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则O处于
钙钛矿( )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料:
)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料:
(1)基态Ca原子的核外电子排布式为___________ 。
(2)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是___________ 。
(3) 的晶胞如图(a)所示,金属离子与氧离子间的作用力为
的晶胞如图(a)所示,金属离子与氧离子间的作用力为___________ , 的配位数是
的配位数是___________ 。 、
、 和有机碱离子
和有机碱离子 ,其晶胞如图(b)所示。其中
,其晶胞如图(b)所示。其中 与图(a)中
与图(a)中___________ 的空间位置相同,有机碱 中,N原子的杂化轨道类型是
中,N原子的杂化轨道类型是___________ ;若晶胞参数为a nm,则晶体密度为___________ g•cm ((列出计算式)。
((列出计算式)。
(1)基态Ca原子的核外电子排布式为
(2)Ti的四卤化物熔点如下表所示,
| 化合物 | ||||
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |


组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


