解答题-实验探究题 适中0.65 引用1 组卷38
用沉淀滴定法 快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
I.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液放在棕色试剂瓶中避光保存备用。
b.配制并标定100mL0.1000mol•L-1NH4SCN标准溶液,备用。
II.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol•L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol•L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如表:
f.数据处理。
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯、玻璃棒、胶头滴管外还有___ 。
(2)滴定应在pH<0.5的条件下进行,其原因是抑制Fe3+的水解。Fe3+的水解离子方程式为:___ 。
(3)测得c(I—)=___ mol•L-1。(结果保留小数点后四位)
(4)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为___ 。
(5)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果___ 。
I.准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液放在棕色试剂瓶中避光保存备用。
b.配制并标定100mL0.1000mol•L-1NH4SCN标准溶液,备用。
II.滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol•L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol•L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如表:
| 实验序号 | 1 | 2 | 3 |
| 消耗NH4SCN标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯、玻璃棒、胶头滴管外还有
(2)滴定应在pH<0.5的条件下进行,其原因是抑制Fe3+的水解。Fe3+的水解离子方程式为:
(3)测得c(I—)=
(4)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为
(5)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果
22-23高二上·黑龙江双鸭山·期中
类题推荐
(一)碘及其化合物广泛用于医药、染料等方面。用沉淀滴定法快速测定NaI等碘化物溶液中
c(I-),实验过程包括准备标准溶液和滴定待测溶液。
一、准备标准溶液
I.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用。
Ⅱ.配制并标定100mL 0.1000mol•L-1 NH4SCN标准溶液,备用。
二、滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol•L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol•L-1 NH4SCN 溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
f.数据处理。
(1)将称得的AgNO3配制成标准溶液,所使用的仪器不包括______
(2)b和c两步操作是否可以颠倒___________ ,说明理由___________ 。
(3)消耗的NH4SCN标准溶液平均体积为___________ mL,计算得c(I-)=___________ mol•L-1;在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为___________ 。
(4)判断下列操作对c(I-)测定结果的影响
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果______
A.偏高 B.偏低 C.无影响 D.无法判断
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果______
A.偏高 B.偏低 C.无影响 D.无法判断
(二)从海水中提取单质碘的一种方法如下图所示:
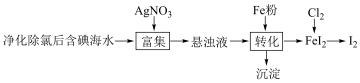
(5)加入铁粉进行转化反应的离子方程式为___________ 。
(6)若反应物用量比 =1.5时,则氧化产物(Fe3+、I2)物质的量之比为______
=1.5时,则氧化产物(Fe3+、I2)物质的量之比为______
c(I-),实验过程包括准备标准溶液和滴定待测溶液。
一、准备标准溶液
I.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用。
Ⅱ.配制并标定100mL 0.1000mol•L-1 NH4SCN标准溶液,备用。
二、滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL0.1000mol•L-1AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.1000mol•L-1 NH4SCN 溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
f.数据处理。
| 实验序号 | 1 | 2 | 3 |
| 消耗NH4SCN标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
(1)将称得的AgNO3配制成标准溶液,所使用的仪器不包括______
| A.烧杯 | B.胶头滴管 | C.容量瓶 | D.量筒 |
(2)b和c两步操作是否可以颠倒
(3)消耗的NH4SCN标准溶液平均体积为
(4)判断下列操作对c(I-)测定结果的影响
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果
A.偏高 B.偏低 C.无影响 D.无法判断
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果
A.偏高 B.偏低 C.无影响 D.无法判断
(二)从海水中提取单质碘的一种方法如下图所示:

(5)加入铁粉进行转化反应的离子方程式为
(6)若反应物用量比
| A.2:1 | B.1:2 | C.1:1 | D.3:2 |
用沉淀滴定法快速测定 等碘化物溶液中
等碘化物溶液中 ,实验过程包括准备标准溶液和滴定待测溶液。
,实验过程包括准备标准溶液和滴定待测溶液。
Ⅰ.准备标准溶液
a.准确称取 基准物
基准物 后,配制成
后,配制成 标准溶液,放在棕色试剂瓶中避光保存,备用。
标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定 标准溶液,备用。
标准溶液,备用。
Ⅱ.滴定的主要步骤
a.取待测NaI溶液 于锥形瓶中。
于锥形瓶中。
b.加入 溶液(过量),使
溶液(过量),使 完全转化为AgI沉淀。
完全转化为AgI沉淀。
c.加入 溶液作指示剂。
溶液作指示剂。
d.用 溶液滴定过量的
溶液滴定过量的 ,使其恰好完全转化为AgSCN白色沉淀后,停止滴定。
,使其恰好完全转化为AgSCN白色沉淀后,停止滴定。
e.重复上述操作两次。三次测定数据如表:
f.数据处理。回答下列问题:
(1)b和c两步操作是否可以颠倒___________ (填“是”或“否”),说明理由___________ 。
(2)所消耗的 标准溶液平均体积为
标准溶液平均体积为___________ mL,测得
___________  。
。
(3)简述滴定终点的判断方法___________ 。
(4)判断下列操作对 测定结果的影响(填“偏高”、“偏低”或“无影响”)
测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制 标准溶液时,烧杯中的溶液有少量溅出,则测定结果
标准溶液时,烧杯中的溶液有少量溅出,则测定结果___________ 。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果___________ 。
Ⅰ.准备标准溶液
a.准确称取
b.配制并标定
Ⅱ.滴定的主要步骤
a.取待测NaI溶液
b.加入
c.加入
d.用
e.重复上述操作两次。三次测定数据如表:
| 实验序号 | 1 | 2 | 3 |
| 消耗NH4SCN标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
(1)b和c两步操作是否可以颠倒
(2)所消耗的
(3)简述滴定终点的判断方法
(4)判断下列操作对
①若在配制
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果
用沉淀滴定法快速测定 等碘化物溶液中
等碘化物溶液中 ,实验过程包括准备标准溶液和滴定待测溶液(已知
,实验过程包括准备标准溶液和滴定待测溶液(已知 为白色沉淀)。
为白色沉淀)。
Ⅰ.准备标准溶液
a.准确称取 基准物
基准物 后,配制成
后,配制成 标准溶液,放在棕色试剂瓶中避光保存,备用。
标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定 标准溶液,备用。
标准溶液,备用。
Ⅱ.滴定待测溶液
a.取待测 溶液
溶液 于锥形瓶中。
于锥形瓶中。
b.加入 溶液(过量),使
溶液(过量),使 完全转化为
完全转化为 沉淀。
沉淀。
c.加入 溶液作指示剂。
溶液作指示剂。
d.用 溶液滴定过量的
溶液滴定过量的 。
。
e.重复上述操作 次,测定数据如表所示。
次,测定数据如表所示。
f.数据处理。
回答下列问题:
(1)将称得的 配制成标准溶液,所使用的玻璃仪器除烧杯、量筒和玻璃棒外,还有两种分别是
配制成标准溶液,所使用的玻璃仪器除烧杯、量筒和玻璃棒外,还有两种分别是___________ 、___________ 。
(2)应在 的条件下进行滴定,其目的是
的条件下进行滴定,其目的是___________ 。
(3)若过程Ⅱ中b和c两步操作颠倒将无法指示反应终点的原因是___________ 。(用离子方程式表示)
(4)达到滴定终点时的现象是___________ 。
(5)由上述实验数据测得
___________  。
。
(6)若在配制 标准溶液时,烧杯中的溶液有少量溅出,则使
标准溶液时,烧杯中的溶液有少量溅出,则使
___________ (填“偏高”“偏低”或“无影响”)。
Ⅰ.准备标准溶液
a.准确称取
b.配制并标定
Ⅱ.滴定待测溶液
a.取待测
b.加入
c.加入
d.用
e.重复上述操作
| 实验序号 | 1 | 2 | 3 |
| 消耗 | 10.24 | 10.02 | 9.98 |
回答下列问题:
(1)将称得的
(2)应在
(3)若过程Ⅱ中b和c两步操作颠倒将无法指示反应终点的原因是
(4)达到滴定终点时的现象是
(5)由上述实验数据测得
(6)若在配制
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


