解答题-工业流程题 适中0.65 引用2 组卷1026
以钡矿粉(主要成份为BaCO3,含有Ca2+、Fe2+、Fe3+、Mg2+等)制备BaCl2·2H2O的流程如下:
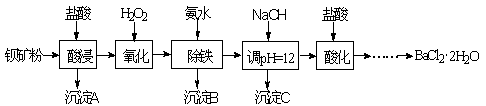
(1)氧化过程主要反应的离子方程式为______ 。
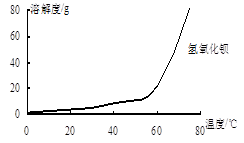
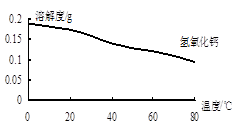
(2)沉淀C的主要成分是Ca(OH)2和______ 。由图可知,为了更好的使Ca2+沉淀,还应采取的措施为______ 。
(3)用BaSO4重量法测定产品纯度的步骤为:
步骤1:准确称取0.4~0.6 g BaCl2·2H2O试样,加入100 ml 水,3 ml 2 mol·L-1的HCl溶液加热溶解。
步骤2:边搅拌,边逐滴加入0.1 mol·L-1 H2SO4溶液。
步骤3:待BaSO4沉降后,______,确认已完全沉淀。
步骤4:过滤,用0.01 mol·L-1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl-为止。
步骤5:将折叠的沉淀滤纸包置于______中,经烘干、炭化、灰化后在800℃灼烧至恒重。称量计算BaCl2·2H2O中Ba2+的含量。
①步骤3所缺的操作为______ 。
②若步骤1称量的样品过少,则在步骤4洗涤时可能造成的影响为______ 。
③步骤5所用瓷质仪器名称为______ 。滤纸灰化时空气要充足,否则BaSO4易被残留的炭还原生成BaS,该反应的化学方程式为______ 。
④有同学认为用K2CrO4代替H2SO4作沉淀剂效果更好,请说明原因______ 。[已知:Ksp(BaSO4)=1.1×10-10 Ksp(BaCrO4)=1.2×10-10]

(1)氧化过程主要反应的离子方程式为
(2)沉淀C的主要成分是Ca(OH)2和


(3)用BaSO4重量法测定产品纯度的步骤为:
步骤1:准确称取0.4~0.6 g BaCl2·2H2O试样,加入100 ml 水,3 ml 2 mol·L-1的HCl溶液加热溶解。
步骤2:边搅拌,边逐滴加入0.1 mol·L-1 H2SO4溶液。
步骤3:待BaSO4沉降后,______,确认已完全沉淀。
步骤4:过滤,用0.01 mol·L-1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl-为止。
步骤5:将折叠的沉淀滤纸包置于______中,经烘干、炭化、灰化后在800℃灼烧至恒重。称量计算BaCl2·2H2O中Ba2+的含量。
①步骤3所缺的操作为
②若步骤1称量的样品过少,则在步骤4洗涤时可能造成的影响为
③步骤5所用瓷质仪器名称为
④有同学认为用K2CrO4代替H2SO4作沉淀剂效果更好,请说明原因
13-14高三上·江苏扬州·阶段练习
类题推荐
工业上制备BaCl2·H2O有如下两种途径:
途径1:以重晶石(主要成分BaSO4)为原料,流程如下:
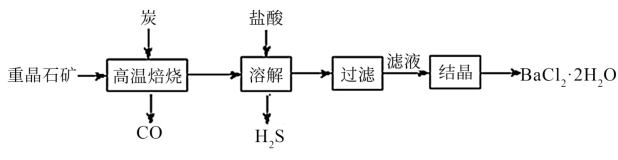
(1)写出“高温焙烧”时反应的化学方程式:____________________________ 。
(2)“高温焙烧”时必须加入过量的炭,同时还要通入空气,其目的是_______________________ 。
途径2:以毒重石(主要成分BaCO3,含Ca2+、Mg2+、Fe3+等杂质)为原料,流程如下:
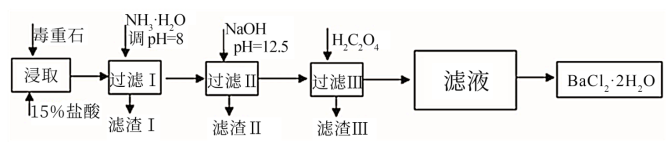
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)过滤Ⅲ所得的滤液经过依次经过_____________ ,_____________ 过滤洗涤后得到Bacl2·2H2O(填操作名称)。
(4)加入NH3·H2O调节pH=8可除去____________ (填离子符号),滤渣Ⅱ中含_________ (填化学式)。加入H2C2O4时应避免过量,原因是________________________ 。
(5)用BaSO4重量法测定产品纯度的步骤为:
准确称取m g BaCl2•2H2O试样,加入100 mL水,3 mL 2 mol•L-1 的HCl溶液加热溶解。边搅拌,边逐滴加入0.1 mol•L-1 H2SO4溶液。待BaSO4完全沉淀并沉降后,过滤,用0.01 mol•L-1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl-为止。将折叠的沉淀滤纸包置于坩埚中经烘干、炭化、灰化后在800℃灼烧至恒重,称量为n g。则BaCl2·2H2O的质量分数为___________ 。
途径1:以重晶石(主要成分BaSO4)为原料,流程如下:

(1)写出“高温焙烧”时反应的化学方程式:
(2)“高温焙烧”时必须加入过量的炭,同时还要通入空气,其目的是
途径2:以毒重石(主要成分BaCO3,含Ca2+、Mg2+、Fe3+等杂质)为原料,流程如下:

已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.7 |
(3)过滤Ⅲ所得的滤液经过依次经过
(4)加入NH3·H2O调节pH=8可除去
(5)用BaSO4重量法测定产品纯度的步骤为:
准确称取m g BaCl2•2H2O试样,加入100 mL水,3 mL 2 mol•L-1 的HCl溶液加热溶解。边搅拌,边逐滴加入0.1 mol•L-1 H2SO4溶液。待BaSO4完全沉淀并沉降后,过滤,用0.01 mol•L-1的稀H2SO4洗涤沉淀3~4次,直至洗涤液中不含Cl-为止。将折叠的沉淀滤纸包置于坩埚中经烘干、炭化、灰化后在800℃灼烧至恒重,称量为n g。则BaCl2·2H2O的质量分数为
工业上制备 BaCl2·2H2O 有如下两种途径。
途径 1:以重晶石(主要成分 BaSO4)为原料,流程如下:
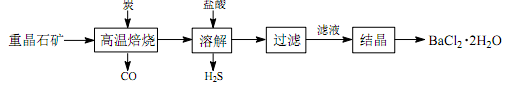
(1)写出“高温焙烧”时反应的化学方程式:_____________________________________ 。
(2)“高温焙烧” 时必须加入过量的炭,同时还要通入空气,其目的是____________ 。
途径 2:以毒重石(主要成分 BaCO3,含 Ca2+、 Mg2+、 Fe3+等杂质)为原料,流程如下:
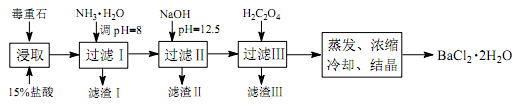
已知: Ksp(BaC2O4)=1.6×10-7, Ksp(CaC2O4)=2.3×10-9
(3)为提高矿石的浸取率,可采取的措施是_________ 。
(4)加入 NH3·H2O 调节 pH=8 可除去____ (填离子符号),滤渣Ⅱ中含_________ (填化学式)。加入 H2C2O4时应避免过量,原因是_________ 。
(5)重量法测定产品纯度的步骤为:
准确称取 m g BaCl2·2H2O 试样,加入 100 mL 水, 用 3 mL 2 mol·L-1 的 HCl 溶液加热溶解。边搅拌,边逐滴加入 0.1 mol·L-1 H2SO4 溶液。待 BaSO4 完全沉降后,过滤,用0.01 mol·L-1 的稀 H2SO4洗涤沉淀 3~4 次,直至洗涤液中不含 Cl-为止。将沉淀置于坩埚中经烘干灼烧至恒重,称量为 n g。则 BaCl2·2H2O 的质量分数为_________ 。
途径 1:以重晶石(主要成分 BaSO4)为原料,流程如下:

(1)写出“高温焙烧”时反应的化学方程式:
(2)“高温焙烧” 时必须加入过量的炭,同时还要通入空气,其目的是
途径 2:以毒重石(主要成分 BaCO3,含 Ca2+、 Mg2+、 Fe3+等杂质)为原料,流程如下:

已知: Ksp(BaC2O4)=1.6×10-7, Ksp(CaC2O4)=2.3×10-9
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的 pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的 pH | 13.9 | 11.1 | 3.7 |
(3)为提高矿石的浸取率,可采取的措施是
(4)加入 NH3·H2O 调节 pH=8 可除去
(5)重量法测定产品纯度的步骤为:
准确称取 m g BaCl2·2H2O 试样,加入 100 mL 水, 用 3 mL 2 mol·L-1 的 HCl 溶液加热溶解。边搅拌,边逐滴加入 0.1 mol·L-1 H2SO4 溶液。待 BaSO4 完全沉降后,过滤,用0.01 mol·L-1 的稀 H2SO4洗涤沉淀 3~4 次,直至洗涤液中不含 Cl-为止。将沉淀置于坩埚中经烘干灼烧至恒重,称量为 n g。则 BaCl2·2H2O 的质量分数为
工业上制备 BaCl2·2H2O有如下两种途径。
途径 1:以重晶石(主要成分BaSO4)为原料,流程如下:
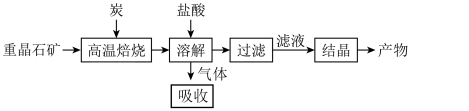
(1)写出“高温焙烧”时反应的化学方程式:_____________________________________ 。
(2)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为_____________ 。
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, =
=___________ 。 [Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10]
途径 2:以毒重石(主要成分BaCO3,含Ca2+、Mg2+、Fe3+等杂质)为原料,流程如下:
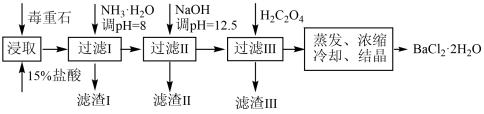
已知:Ksp(BaC2O4)=1.6×10-7, Ksp(CaC2O4)=2.3×10-9
(4)为提高矿石的浸取率,可采取的措施是_________ 。
(5)加入 NH3·H2O 调节 pH=8 可除去___________ (填离子符号),滤渣Ⅱ中含_________ (填化学式)。加入 H2C2O4时应避免过量,原因是_________ 。
(6)重量法测定产品纯度的步骤为:准确称取 m g BaCl2·2H2O试样,加入100 mL水, 用3 mL 2 mol·L-1的 HCl溶液加热溶解。边搅拌,边逐滴加入0.1 mol·L-1 H2SO4 溶液。待BaSO4完全沉降后,过滤,用0.01 mol·L-1的稀H2SO4洗涤沉淀 3~4 次,直至洗涤液中不含Cl-为止。将沉淀置于坩埚中经烘干灼烧至恒重,称量为n g。则BaCl2·2H2O的质量分数为_________ 。
(7)20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g·L-1)如图所示。下列叙述正确的是_______________
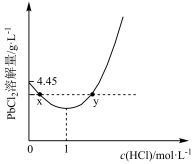
A.盐酸浓度越大,Ksp(PbCl2)越大
B.PbCl2能与一定浓度的盐酸反应
C.x、y两点对应的溶液中c(Pb2+)相等
D.往含Pb2+的溶液中加入过量浓盐酸,可将Pb2+完全转化为PbCl2(s)
途径 1:以重晶石(主要成分BaSO4)为原料,流程如下:

(1)写出“高温焙烧”时反应的化学方程式:
(2)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为
(3)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,
途径 2:以毒重石(主要成分BaCO3,含Ca2+、Mg2+、Fe3+等杂质)为原料,流程如下:

已知:Ksp(BaC2O4)=1.6×10-7, Ksp(CaC2O4)=2.3×10-9
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的 pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的 pH | 13.9 | 11.1 | 3.7 |
(4)为提高矿石的浸取率,可采取的措施是
(5)加入 NH3·H2O 调节 pH=8 可除去
(6)重量法测定产品纯度的步骤为:准确称取 m g BaCl2·2H2O试样,加入100 mL水, 用3 mL 2 mol·L-1的 HCl溶液加热溶解。边搅拌,边逐滴加入0.1 mol·L-1 H2SO4 溶液。待BaSO4完全沉降后,过滤,用0.01 mol·L-1的稀H2SO4洗涤沉淀 3~4 次,直至洗涤液中不含Cl-为止。将沉淀置于坩埚中经烘干灼烧至恒重,称量为n g。则BaCl2·2H2O的质量分数为
(7)20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g·L-1)如图所示。下列叙述正确的是

A.盐酸浓度越大,Ksp(PbCl2)越大
B.PbCl2能与一定浓度的盐酸反应
C.x、y两点对应的溶液中c(Pb2+)相等
D.往含Pb2+的溶液中加入过量浓盐酸,可将Pb2+完全转化为PbCl2(s)
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


