解答题-实验探究题 适中0.65 引用1 组卷174
按要求完成下列填空,
(1)配制240mL4.0mol•L-1NaOH溶液的实验步骤如下:
a.计算需要氢氧化钠固体的质量;
b.用滤纸称量氢氧化钠固体
c.用适量的蒸馏水溶解称量好的氢氧化钠固体,直接注入容量瓶;
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液也注入容量瓶,轻轻摇动容量瓶使溶液混合均匀;
e.继续向容量瓶中加蒸馏水至刻度线下1mm~2mm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
f.盖好瓶塞,反复左右颠倒,摇匀;
g.装瓶贴签。
①所需称量的氢氧化钠固体的质量是_____ 。
②配制上述溶液的操作正确的是_____ (填序号)。
③在配制过程中,其他操作均正确,下列操作能引起所得溶液浓度偏高的是_____ (填序号)。
A.定容时,俯视刻度线
B.定容摇匀后,发现液面低于刻度线,又用胶头滴管滴加蒸馏水至刻度线
C.转移前,发现容量瓶内含有少量蒸馏水
D.称量时使用的砝码生锈
(2)已知该水样中只可能含有K+、Mg2+、Cu2+、Ag+、Ca2+、 、
、 、Cl-中的若干种离子,该小组同学取100mL水样进行实验;向样品中先滴加氯化钡溶液,再滴加1mol•L-1盐酸,实验过程中沉淀质量的变化如图所示。
、Cl-中的若干种离子,该小组同学取100mL水样进行实验;向样品中先滴加氯化钡溶液,再滴加1mol•L-1盐酸,实验过程中沉淀质量的变化如图所示。
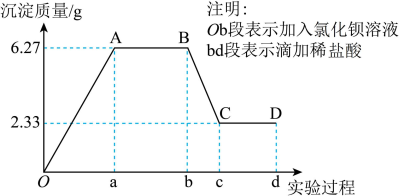
BC段消耗盐酸体积为_____ ,若检测得到c(K+)=0.7mol•L-1,则水样中存在的离子为_____ 。
(3)在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
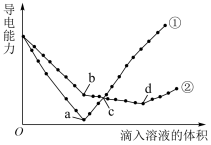
下列分析正确的是_____ 。
(4)将0.24gMg和0.27gAl的混合物投入到100mL1mol/L的盐酸中,充分反应后固体完全溶解。向所得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全,需要NaOH溶液的体积为_____ mL。
(1)配制240mL4.0mol•L-1NaOH溶液的实验步骤如下:
a.计算需要氢氧化钠固体的质量;
b.用滤纸称量氢氧化钠固体
c.用适量的蒸馏水溶解称量好的氢氧化钠固体,直接注入容量瓶;
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液也注入容量瓶,轻轻摇动容量瓶使溶液混合均匀;
e.继续向容量瓶中加蒸馏水至刻度线下1mm~2mm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
f.盖好瓶塞,反复左右颠倒,摇匀;
g.装瓶贴签。
①所需称量的氢氧化钠固体的质量是
②配制上述溶液的操作正确的是
③在配制过程中,其他操作均正确,下列操作能引起所得溶液浓度偏高的是
A.定容时,俯视刻度线
B.定容摇匀后,发现液面低于刻度线,又用胶头滴管滴加蒸馏水至刻度线
C.转移前,发现容量瓶内含有少量蒸馏水
D.称量时使用的砝码生锈
(2)已知该水样中只可能含有K+、Mg2+、Cu2+、Ag+、Ca2+、

BC段消耗盐酸体积为
(3)在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。

下列分析正确的是
| A.①代表滴加H2SO4溶液的变化曲线 | B.b-d的反应为H++OH-=H2O |
| C.a、d两点对应的溶液均显中性 | D.H+导电能力比Na+弱 |
22-23高一上·湖北武汉·阶段练习
知识点:物质水溶液的导电性配制一定物质的量浓度的溶液的步骤、操作配制一定物质的量浓度的溶液实验的误差分析探究物质组成或测量物质的含量 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
配制250ml 4.0mol•L-1NaOH溶液的实验步骤如下:
a.计算需要氢氧化钠固体的质量;
b.用滤纸称量氢氧化钠固体
c.用适量的蒸馏水溶解称量好的氢氧化钠固体,直接注入容量瓶;
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液也注入容量瓶,轻轻摇动容量瓶使溶液混合均匀;
e.继续向容量瓶中加蒸馏水至刻度线下1mm~2mm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
f.盖好瓶塞,反复左右颠倒,摇匀;
g.装瓶贴签。
(1)所需称量的氢氧化钠固体的质量是_______ 。
(2)配制上述溶液的操作正确的是_______ (填序号)。
(3)在配制过程中,其他操作均正确,下列操作能引起所得溶液浓度偏高的是_______(填序号)。
a.计算需要氢氧化钠固体的质量;
b.用滤纸称量氢氧化钠固体
c.用适量的蒸馏水溶解称量好的氢氧化钠固体,直接注入容量瓶;
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液也注入容量瓶,轻轻摇动容量瓶使溶液混合均匀;
e.继续向容量瓶中加蒸馏水至刻度线下1mm~2mm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
f.盖好瓶塞,反复左右颠倒,摇匀;
g.装瓶贴签。
(1)所需称量的氢氧化钠固体的质量是
(2)配制上述溶液的操作正确的是
(3)在配制过程中,其他操作均正确,下列操作能引起所得溶液浓度偏高的是_______(填序号)。
| A.定容时,俯视刻度线 |
| B.定容摇匀后,发现液面低于刻度线,又用胶头滴管滴加蒸馏水至刻度线 |
| C.转移前,发现容量瓶内含有少量蒸馏水 |
| D.称量时使用的砝码生锈 |
按要求完成下列填空:
1.配制 溶液的实验步骤如下:
溶液的实验步骤如下:
a.计算需要氢氧化钠固体的质量
b.用滤纸称量氢氧化钠固体;
c.用适量的蒸馏水溶解称量好的氢氧化钠固体,直接注入容量瓶;
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液也注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
e.继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切:
f.盖好瓶塞,反复上下颠倒,摇匀;
g.将配制好的溶液倒入试剂瓶中,并贴好标签。
(1)下图所示的仪器中,配制溶液肯定不需要的是___________ (填序号),配制上述溶液还需用到的玻璃仪器有烧杯、玻璃棒和___________ (填仪器名称)。

(2)所需称量的氢氧化钠固体的质量是___________ 。
(3)配制上述溶液的操作不正确的是___________ (填序号)。
(4)配制过程中,其他操作均正确,下列能引起所得溶液浓度偏高的是___________(填序号)。
II.化学实验和科学研究中常需要用一定溶质质量分数的溶液配制一定物质的量浓度的溶液。
(5)现用质量分数为98%、密度为 的浓硫酸来配制500mL、
的浓硫酸来配制500mL、 的稀硫酸。计算所需浓硫酸的体积为
的稀硫酸。计算所需浓硫酸的体积为___________ mL(保留1位小数),现有①10mL②25mL③50mL④100mL四种规格的量筒,你选用的量筒是___________ (填代号)。
(6)在实验中其他操作均正确,若用量筒量取浓硫酸时仰视刻度线,则所配溶液浓度___________ (填“偏大”、“偏小”或“无影响”)。
1.配制
a.计算需要氢氧化钠固体的质量
b.用滤纸称量氢氧化钠固体;
c.用适量的蒸馏水溶解称量好的氢氧化钠固体,直接注入容量瓶;
d.用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液也注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
e.继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切:
f.盖好瓶塞,反复上下颠倒,摇匀;
g.将配制好的溶液倒入试剂瓶中,并贴好标签。
(1)下图所示的仪器中,配制溶液肯定不需要的是

(2)所需称量的氢氧化钠固体的质量是
(3)配制上述溶液的操作不正确的是
(4)配制过程中,其他操作均正确,下列能引起所得溶液浓度偏高的是___________(填序号)。
| A.定容时,俯视刻度线 |
| B.定容摇匀后,发现液面低于刻度线,又用胶头滴管滴加蒸馏水至刻度线 |
| C.转移前,发现容量瓶内含有少量蒸馏水 |
| D.称量时使用的砝码生锈 |
II.化学实验和科学研究中常需要用一定溶质质量分数的溶液配制一定物质的量浓度的溶液。
(5)现用质量分数为98%、密度为
(6)在实验中其他操作均正确,若用量筒量取浓硫酸时仰视刻度线,则所配溶液浓度
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


