填空题 适中0.65 引用1 组卷43
运用化学反应原理研究化学反应有重要意义。
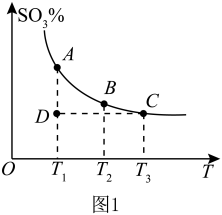
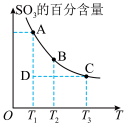
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。
2SO3(g),混合体系中SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。
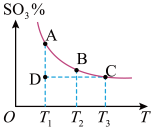
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡_______ (填“向左”“向右”或“不”)移动。
②若反应进行到状态D时,v(逆)_______ (填“>”“<”或“=”)v(正)
③平衡常数K(A)_______ K(C)(填“>”“<”或“=”)
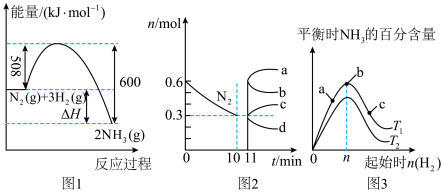
(2)课本里介绍的合成氨技术叫哈伯法:N2(g)+3H2(g) 2NH3(g) ΔH<0,应用此法反应达到平衡时反应物的转化率不高。
2NH3(g) ΔH<0,应用此法反应达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是_______ (填编号)。
A.使用更高效的催化剂 B.升高温度
C.及时分离出氨气 D.充入氮气,增大氮气的浓度(保持容器体积不变)
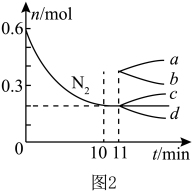
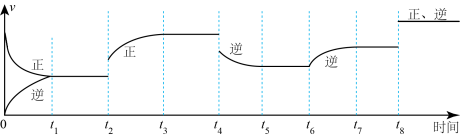
②若在某温度下,2L的密闭容器中发生合成氨的反应,如图表示N2的物质的量随时间的变化曲线。从第11min起,升高温度,则n(N2)的变化曲线为_______ (填编号)。

(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)

①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡
②若反应进行到状态D时,v(逆)
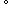
③平衡常数K(A)
(2)课本里介绍的合成氨技术叫哈伯法:N2(g)+3H2(g)
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是
A.使用更高效的催化剂 B.升高温度
C.及时分离出氨气 D.充入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下,2L的密闭容器中发生合成氨的反应,如图表示N2的物质的量随时间的变化曲线。从第11min起,升高温度,则n(N2)的变化曲线为

22-23高二上·安徽亳州·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网