解答题-原理综合题 适中0.65 引用2 组卷334
将二氧化碳加氢转化为高附加值的化学品或液体燃料是二氧化碳资源化利用的有效方法,其中转换为甲醇被认为是最可能的利用路径,主要涉及反应如下:
反应I:

反应II:

请回答下列问题:
(1)已知 的燃烧热
的燃烧热 和CO的燃烧热
和CO的燃烧热 ,水的汽化热(1mol
,水的汽化热(1mol 从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的
从液体汽化为气体所需要吸收的热量)为40.8kJ/mol,则反应II的
_______ 。
(2) 和
和 在某NiO支撑的
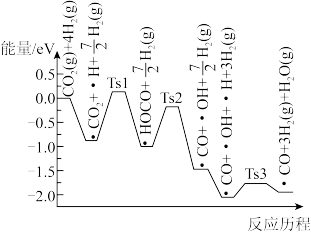
在某NiO支撑的 表面的反应历程如下图所示。(TS表示过渡态)
表面的反应历程如下图所示。(TS表示过渡态)
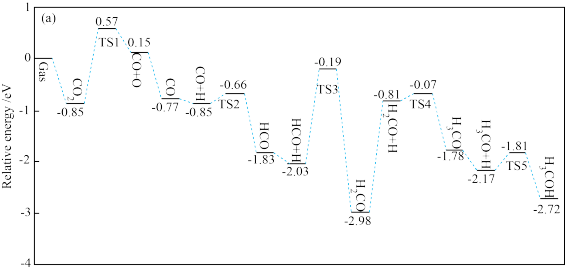
决定总反应速率的步骤的反应方程式为_______ ,该步骤的活化能
_______ eV。
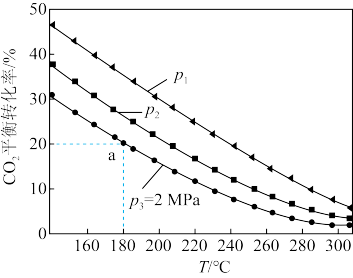
(3)恒定压强P下,体积比1:3的 和
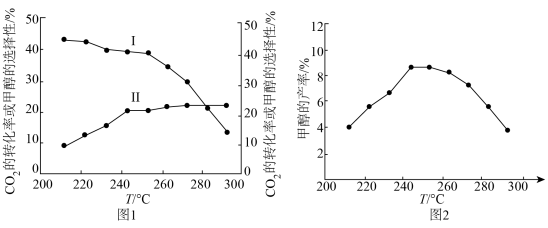
和 发生反应I、反应II,反应相同时间,测得不同温度下
发生反应I、反应II,反应相同时间,测得不同温度下 的转化率和
的转化率和 的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态
的选择性如下图中实验值所示。图中平衡值表示相同条件下平衡状态 的转化率和
的转化率和 的选择性随温度的变化[
的选择性随温度的变化[ 的选择性
的选择性 ]
]
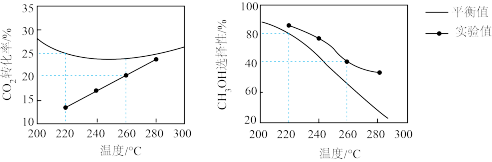
①当温度高于260℃时,二氧化碳的平衡转化率随温度升高而增大的原因是_______ 。
②260℃时,甲醇产率的实验值是_______ 。220℃-260℃甲醇的选择性随温度升高降低的原因是_______ 。
③220℃时,反应II的化学平衡常数
_______ 。
反应I:
反应II:
请回答下列问题:
(1)已知
(2)

决定总反应速率的步骤的反应方程式为
(3)恒定压强P下,体积比1:3的

①当温度高于260℃时,二氧化碳的平衡转化率随温度升高而增大的原因是
②260℃时,甲醇产率的实验值是
③220℃时,反应II的化学平衡常数
22-23高三上·广东·阶段练习
类题推荐
CO2的转化和利用是实现碳中和的有效途径,其中CO2转化为CH3OH被认为是最可能利用的路径,该路径涉及反应如下:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.01kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.01kJ•mol-1
反应II:CO2(g)+H2(g) CO(g)+H2O(g) △H2>0
CO(g)+H2O(g) △H2>0
请回答下列问题:
(1)若利用反应I计算反应II的反应热△H2,还需要知道一个化学反应的△H,写出该反应的化学方程式_______ 。
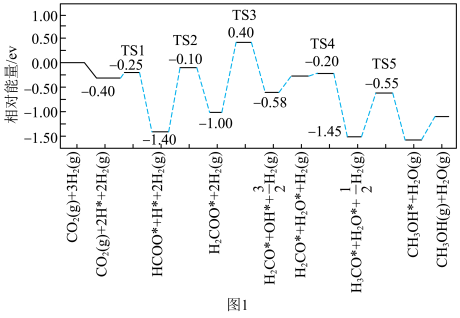
(2)在催化剂条件下,反应I的反应机理和相对能量变化如图1(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。_______ 。
(3)在恒温恒压(260℃,1.8MPa)下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如表。
已知:
i.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
ii.CH3OH的选择性= ×100%
×100%
①在普通反应器(A)中,下列能作为反应I和反应II均达到平衡状态的判断判据是_______ (填字母)。
A.气体压强不再变化
B.气体的密度不再改变
C.v正(CO2)=3v逆(H2)
D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是_______ ;在反应器(B)中,CO2的平衡转化率明显高于反应器(A),可能的原因是______ 。
③若反应器(A)中初始时n(CO2)=1mol,反应I从开始到平衡态的平均反应速率v(CH3OH)=_______ mol•s-1;反应II的化学平衡常数Kp(II)=_______ (列出化简后的计算式即可)。
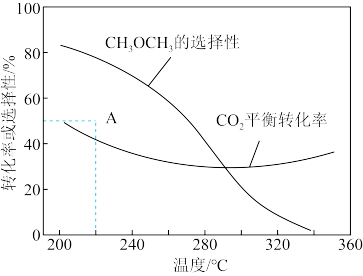
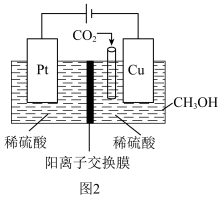
(4)近年来,有研究人员用CO2通过电催化生成CH3OH,实现CO2的回收利用,其工作原理如图2所示,请写出Cu电极上的电极反应:_______ 。
反应I:CO2(g)+3H2(g)
反应II:CO2(g)+H2(g)
请回答下列问题:
(1)若利用反应I计算反应II的反应热△H2,还需要知道一个化学反应的△H,写出该反应的化学方程式
(2)在催化剂条件下,反应I的反应机理和相对能量变化如图1(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
(3)在恒温恒压(260℃,1.8MPa)下,CO2和H2按体积比1:3分别在普通反应器(A)和分子筛膜催化反应器(B)中反应,测得相关数据如表。
| 反应器 | CO2平衡转化率 | 甲醇的选择性 | 达到平衡时间/s |
| 普通反应器(A) | 25.0% | 80.0% | 10.0 |
| 分子筛膜催化反应器(B) | >25.0% | 100.0% | 8.0 |
i.分子筛膜催化反应器(B)具有催化反应、分离出部分水蒸气的双重功能;
ii.CH3OH的选择性=
①在普通反应器(A)中,下列能作为反应I和反应II均达到平衡状态的判断判据是
A.气体压强不再变化
B.气体的密度不再改变
C.v正(CO2)=3v逆(H2)
D.各物质浓度比不再改变
②平衡状态下,反应器(A)中,甲醇的选择性随温度升高而降低,可能的原因是
③若反应器(A)中初始时n(CO2)=1mol,反应I从开始到平衡态的平均反应速率v(CH3OH)=
(4)近年来,有研究人员用CO2通过电催化生成CH3OH,实现CO2的回收利用,其工作原理如图2所示,请写出Cu电极上的电极反应:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网