解答题-实验探究题 较难0.4 引用4 组卷1181
对甲基苯胺可用对硝基甲苯作原料在一定条件制得。主要反应及装置如下:

主要反应物和产物的物理性质见下表:
实验步骤如下:
①向三颈烧瓶中加入50mL稀盐酸、10.7mL(13.7g)对硝基甲苯和适量铁粉,维持瓶内温度在80℃左右,同时搅拌回流、使其充分反应;
②调节pH=7~8,再逐滴加入30mL苯充分混合;
③抽滤得到固体,将滤液静置、分液得液体M;
④向M中滴加盐酸,振荡、静置、分液,向下层液体中加入NaOH溶液,充分振荡、静置;
⑤抽滤得固体,将其洗涤、干燥得6.1g产品。
回答下列问题:
(1)主要反应装置如图,a处缺少的装置是_______ (填仪器名称),实验步骤③和④的分液操作中使用到下列仪器中的_______ (填标号)。
a.烧杯 b.漏斗 c.玻璃棒 d.铁架台
(2)步骤②中用5%的碳酸钠溶液调pH=7~8的目的之一是使Fe3+转化为氢氧化铁沉淀,另一个目的是_______ 。
(3)步骤③中液体M是分液时的_______ 层(填“上”或“下”)液体,加入盐酸的作用是_______ 。
(4)步骤④中加入氢氧化钠溶液后发生反应的离子方程式有_______ 。
(5)步骤⑤中,以下洗涤剂中最合适的是_______ (填标号)。
a.乙醇 b.蒸馏水 c.HCl溶液 d.NaOH溶液
(6)本实验的产率是_______ %。(计算结果保留一位小数)

主要反应物和产物的物理性质见下表:
| 化合物 | 溶解性 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
| 对硝基甲苯 | 不溶于水,溶于乙醇、苯 | 51.4 | 237.7 | 1.286 |
| 对甲基苯胺 | 微溶于水,易溶于乙醇、苯 | 43~45 | 200~202 | 1.046 |
| 对甲基苯胺盐酸盐 | 易溶于水,不溶于乙醇、苯 | 243~245 | -- | -- |
| 苯 | 不溶于水,溶于乙醇 | 5.5 | 80.1 | 0.874 |
①向三颈烧瓶中加入50mL稀盐酸、10.7mL(13.7g)对硝基甲苯和适量铁粉,维持瓶内温度在80℃左右,同时搅拌回流、使其充分反应;
②调节pH=7~8,再逐滴加入30mL苯充分混合;
③抽滤得到固体,将滤液静置、分液得液体M;
④向M中滴加盐酸,振荡、静置、分液,向下层液体中加入NaOH溶液,充分振荡、静置;
⑤抽滤得固体,将其洗涤、干燥得6.1g产品。
回答下列问题:
(1)主要反应装置如图,a处缺少的装置是
a.烧杯 b.漏斗 c.玻璃棒 d.铁架台
(2)步骤②中用5%的碳酸钠溶液调pH=7~8的目的之一是使Fe3+转化为氢氧化铁沉淀,另一个目的是
(3)步骤③中液体M是分液时的
(4)步骤④中加入氢氧化钠溶液后发生反应的离子方程式有
(5)步骤⑤中,以下洗涤剂中最合适的是
a.乙醇 b.蒸馏水 c.HCl溶液 d.NaOH溶液
(6)本实验的产率是
2021·四川绵阳·模拟预测
类题推荐
对甲基苯胺可用对硝基甲苯在酸性条件下用铁粉还原制得:
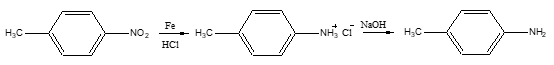
主要反应物和产物的物理性质见下表:
实验流程如下:
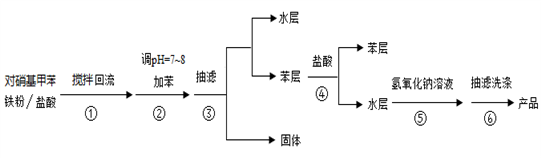
请回答下列问题:
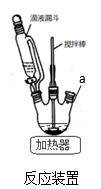
(1)反应装置如图,a处缺少一装置_____________ (填仪器名称)
(2)步骤②中加苯的作用是_____________ ,步骤②中用5%碳酸钠溶液调pH=7~8的原因_________
(3)步骤③得到的固体物质为_________
(4)步骤④中加入盐酸的作用是_____________
(5)步骤⑤中通过加入氢氧化钠溶液使对甲基苯胺结晶析出的原理为_____________
(6)步骤⑥中,以下洗涤剂最合适的是_____________
A. 蒸馏水 B.乙醇 C.NaOH溶液 D.HCl溶液

主要反应物和产物的物理性质见下表:
| 化合物 | 物质状态 | 溶解性 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
| 对硝基甲苯 | 浅黄色晶体 | 不溶于水,溶于乙醇、苯 | 51.4 | 237.7 | 1.286 |
| 对甲基苯胺 | 白色片状晶体 | 微溶于水,易溶于乙醇、苯 | 43~45 | 200~202 | 1.046 |
| 对甲基苯胺盐酸盐 | 白色晶体 | 易溶于水,不溶于乙醇、苯 | 243~245 | —— | —— |
| 苯 | 无色液体 | 不溶于水,溶于乙醇 | 5.5 | 80.1 | 0.874 |

请回答下列问题:
(1)反应装置如图,a处缺少一装置

(2)步骤②中加苯的作用是
(3)步骤③得到的固体物质为
(4)步骤④中加入盐酸的作用是
(5)步骤⑤中通过加入氢氧化钠溶液使对甲基苯胺结晶析出的原理为
(6)步骤⑥中,以下洗涤剂最合适的是
A. 蒸馏水 B.乙醇 C.NaOH溶液 D.HCl溶液
苯佐卡因(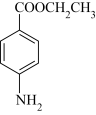 )是一种常用镇痛药,难溶于水,易溶于醇、醚类。实验室里可由对氨基苯甲酸(
)是一种常用镇痛药,难溶于水,易溶于醇、醚类。实验室里可由对氨基苯甲酸(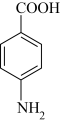 )与乙醇反应合成。
)与乙醇反应合成。
已知:几种物质的某些数据如下。
回答下列问题:
I.合成对氨基苯甲酸
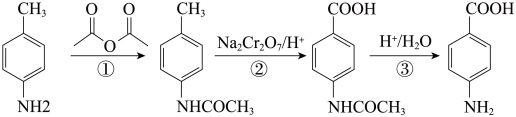
(1)对氨基苯甲酸在一定条件下可生成高分子化合物,该反应的化学方程式为_______ 。
(2)设计步骤“①”和“③”的目的为_______ 。
II.制备苯佐卡因
①在圆底烧瓶中加入5.48g对氨基苯甲酸和60mL无水乙醇,振荡溶解,再加入8mL浓硫酸,将反应混合物在80℃水浴中加热1h,并不时振荡;
②液体冷却后将反应物转移到烧杯中,分批加入Na2CO3溶液(10%)至pH=9;
③将液体转移至分液漏斗中,用乙醚分两次萃取;
④向乙醚层加入无水硫酸镁,滤去固体,进行操作a,冷却结晶,最终得到2.48g产物。
(3)仪器A的名称为_______ ,作用是_______ 。

(4)分液漏斗使用之前必须进行的操作为_______ ,分液操作中,应充分振荡,然后静置,待分层后_______ (填标号)。
A.直接将有机层从分液漏斗上口倒出
B.直接将有机层从分液漏斗下口放出
C先将水层从分液漏斗的下口放出,再将有机层从下口放出
D.先将水层从分液漏斗的下口放出,再将有机层从上口倒出
(5)“步骤④”中无水硫酸镁的作用为_______ ,“操作a”为_______ 。
(6)本实验中苯佐卡因的产率为_______ %(结果保留一位小数)。
 )是一种常用镇痛药,难溶于水,易溶于醇、醚类。实验室里可由对氨基苯甲酸(
)是一种常用镇痛药,难溶于水,易溶于醇、醚类。实验室里可由对氨基苯甲酸( )与乙醇反应合成。
)与乙醇反应合成。已知:几种物质的某些数据如下。
| 试剂 | 相对分子质量 | 密度/g·cm-3 | 熔点/℃ | 沸点/℃ |
| 乙醇 | 46 | 0.79 | 78.5 | |
| 对氨基苯甲酸 | 137 | 188 | 399.9 | |
| 对氨基萃甲酸乙酯 | 165 | 90 | 172 | |
| 乙醚 | 74 | 0.714 | 34.5 |
I.合成对氨基苯甲酸

(1)对氨基苯甲酸在一定条件下可生成高分子化合物,该反应的化学方程式为
(2)设计步骤“①”和“③”的目的为
II.制备苯佐卡因
①在圆底烧瓶中加入5.48g对氨基苯甲酸和60mL无水乙醇,振荡溶解,再加入8mL浓硫酸,将反应混合物在80℃水浴中加热1h,并不时振荡;
②液体冷却后将反应物转移到烧杯中,分批加入Na2CO3溶液(10%)至pH=9;
③将液体转移至分液漏斗中,用乙醚分两次萃取;
④向乙醚层加入无水硫酸镁,滤去固体,进行操作a,冷却结晶,最终得到2.48g产物。
(3)仪器A的名称为

(4)分液漏斗使用之前必须进行的操作为
A.直接将有机层从分液漏斗上口倒出
B.直接将有机层从分液漏斗下口放出
C先将水层从分液漏斗的下口放出,再将有机层从下口放出
D.先将水层从分液漏斗的下口放出,再将有机层从上口倒出
(5)“步骤④”中无水硫酸镁的作用为
(6)本实验中苯佐卡因的产率为
某科学小组制备硝基苯的实验装置如下,有关数据列如下表:
实验步骤如下:
取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制成混和酸,将混合酸小心地加入B中。把0.2mol(15.6g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:
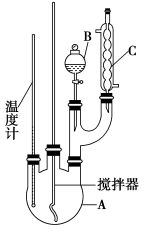
(1)图中B仪器的名称___________ ,图中装置C的作用是___________ 。
(2)制备硝基苯的化学方程式___________ 。
(3)为了使反应在50~60℃下进行,常用的加热方式是___________ 。反应结束并冷却至室温后A中液体就是粗硝基苯,粗硝基苯呈黄色的原因是溶有的浓硝酸分解生成___________ ,实验室常用氢氧化钠溶液除去该有色物质生成两种盐,涉及的离子方程式为___________ 。
(4)将粗产品置于分液漏斗中加水,振荡后静置,产物应在___________ (填“上”或“下”)层,步骤中加入的无水CaCl2的作用是___________ ,若实验过程中省略该步操作,实验的产率___________ (填“偏高”“偏低”或“不变”)。
(5)本实验所得到的硝基苯产率是___________ 。(结果保留3位有效数字)
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g∙cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 不溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
取100mL烧杯,用20mL浓硫酸与足量浓硝酸配制成混和酸,将混合酸小心地加入B中。把0.2mol(15.6g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,使溶液混和均匀。在50~60℃下发生反应,直至反应结束。
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g。
回答下列问题:

(1)图中B仪器的名称
(2)制备硝基苯的化学方程式
(3)为了使反应在50~60℃下进行,常用的加热方式是
(4)将粗产品置于分液漏斗中加水,振荡后静置,产物应在
(5)本实验所得到的硝基苯产率是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


