填空题 适中0.65 引用1 组卷84
请你查找相关数据,回答下列问题。
(1) 、
、 、
、 三种一元酸的酸性由强到弱的顺序是
三种一元酸的酸性由强到弱的顺序是_______ 。
(2)相同物质的量浓度的 溶液、
溶液、 溶液、
溶液、 溶液的
溶液的 由大到小的顺序是
由大到小的顺序是_______ 。
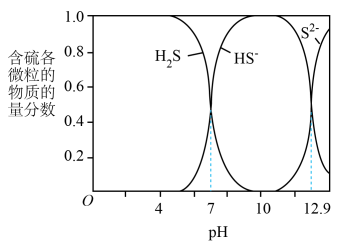
(3) 溶液中含有
溶液中含有_____ 微粒?请将溶液中各种离子的浓度按由大到小的顺序排列_____ 。
(4)向 溶液中加入少量盐酸,溶液中各种微粒的浓度将如何变化
溶液中加入少量盐酸,溶液中各种微粒的浓度将如何变化_____ ?
(5)加热 溶液,溶液中各种微粒的浓度将如何变化?
溶液,溶液中各种微粒的浓度将如何变化?_____
(1)
(2)相同物质的量浓度的
(3)
(4)向
(5)加热
20-21高二·全国·课时练习
类题推荐
电离平衡常数是衡量弱电解质电离程度的物理量。已知:
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为________ (用化学式表示)。
(2)向NaCN溶液中通入少量的CO2,发生反应的化学方程式为_____________ 。
(3)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________ mol·L-1(填精确值),c(CH3COO-)/c(CH3COOH)=________ 。
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(1)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,三溶液的pH由大到小的顺序为
(2)向NaCN溶液中通入少量的CO2,发生反应的化学方程式为
(3)25 ℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=
常温下,常见的弱酸的电离平衡常数如下表所示:
(1)将少量CO2气体通入NaClO溶液中的离子方程式为_______ 。
(2)常温下,某氨水的浓度为2.0 mol·L-1
①该溶液中的c(OH-)=_______ 。
②把SO2通入氨水中,当溶液呈中性时, =
=_______ 。
(3)已知常温下0.1 mol·L-1的CH3COONa和NaHCO3的pH分别为8.9和8.3,而水解常数Kh(CH3COO-)<Kh( ),则NaHCO3溶液pH更小的原因是
),则NaHCO3溶液pH更小的原因是_______ 。
| 酸 | CH3COOH | HClO | NH3·H2O | H2SO3 | H2CO3 |
| 电离平衡常数 | 1.75×10-5 | 4.0×10-8 | 1.8×10-5 | Ka1=1.4×10-2 Ka2=6.0×10-8 | Ka1=4.5×10-7 Ka2=4.7×10-11 |
(2)常温下,某氨水的浓度为2.0 mol·L-1
①该溶液中的c(OH-)=
②把SO2通入氨水中,当溶液呈中性时,
(3)已知常温下0.1 mol·L-1的CH3COONa和NaHCO3的pH分别为8.9和8.3,而水解常数Kh(CH3COO-)<Kh(
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网