单选题 适中0.65 引用1 组卷223
已知:2H2O(l)=2H2(g)+O2(g) △H=+571.0kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=+313.2kJ/mol
过程II:……
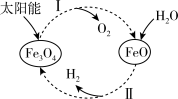
下列说法不正确的是
过程I:2Fe3O4(s)=6FeO(s)+O2(g) △H=+313.2kJ/mol
过程II:……

下列说法不正确的是
| A.铁氧化物循环制H2的方法相较于电解法成本更低 |
| B.过程II热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) △H=+128.9kJ/mol |
| C.过程I、II中能量转化的形式依次是:太阳能→化学能→热能 |
| D.过程I中正反应的活化能大于逆反应的活化能 |
22-23高二上·四川成都·期中
类题推荐
已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.6kJ·mol-1。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如下:
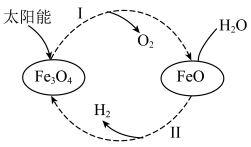
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ·mol
过程Ⅱ:……
下列说法不正确的是

过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ·mol
过程Ⅱ:……
下列说法不正确的是
| A.该过程能量转化形式是太阳能→化学能 |
| B.过程Ⅱ的热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol-1 |
| C.氢气的燃烧热ΔH=-285.8kJ·mol-1 |
| D.过程Ⅰ每转移2mol电子吸收313.2kJ热量 |
已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.6kJ·mol-1.以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如图:
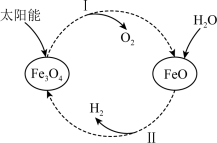
过程Ⅰ:……
过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol-1
下列说法正确的是

过程Ⅰ:……
过程Ⅱ:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol-1
下列说法正确的是
| A.该过程能量转化形式是太阳能→化学能→热能 |
| B.过程Ⅰ热化学方程式为:Fe3O4(s)=3FeO(s)+ |
| C.氢气的燃烧热为ΔH=-285.8 kJ·mol-1 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.6kJ·mol-1。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的图示与过程如下:
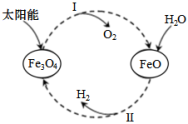
过程I:……
过程II:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol﹣1
下列说法错误的是

过程I:……
过程II:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+129.2kJ·mol﹣1
下列说法错误的是
| A.该过程I能量转化形式是太阳能→化学能 |
| B.过程I热化学方程式为:Fe3O4(s)=3FeO(s)+ |
| C.氢气的燃烧热为ΔH=﹣285.8 kJ·mol﹣1 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


