解答题-实验探究题 较易0.85 引用1 组卷258
某实验兴趣小组同学进行胶体的制备及性质实验,回答下列问题。
I、氢氧化铁胶体的制备和性质
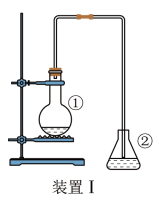
(1)图中仪器a的名称为___________ 。
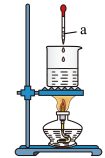
(2)①设计实验证明获得了氢氧化铁胶体___________ 。
②烧杯中发生反应的化学方程式为___________ 。
II、AgI是难溶于水的黄色沉淀,在一定条件下也可以形成胶体。兴趣小组设计如下实验探究某种条件对AgI胶体粒子所带电性的影响:
实验①:将稀AgNO3溶液逐滴加入过量的稀KI溶液中,得到AgI胶体I;
实验②:将稀KI溶液逐滴加入过量的稀AgNO3溶液中,得到AgI胶体II;
实验③:将提纯后的AgI胶体I与AgI胶体II进行混合,出现了黄色沉淀。
完成下列填空:
(3)写出制备AgI胶体I的离子方程式___________ 。
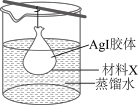
(4)提纯AI胶体的方法如图所示。
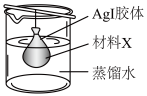
材料X为___________ 。用该法提纯AgI胶体II,进入蒸馏水中而被除去的离子有___________ (写离子符号,写三种)。
(5)本实验的探究结论是制备AgI胶体时反应物的用量对胶体粒子所带电性___________ (选填“有”或“无”)影响。简述作出此判断的理由___________ 。
I、氢氧化铁胶体的制备和性质
(1)图中仪器a的名称为

(2)①设计实验证明获得了氢氧化铁胶体
②烧杯中发生反应的化学方程式为
II、AgI是难溶于水的黄色沉淀,在一定条件下也可以形成胶体。兴趣小组设计如下实验探究某种条件对AgI胶体粒子所带电性的影响:
实验①:将稀AgNO3溶液逐滴加入过量的稀KI溶液中,得到AgI胶体I;
实验②:将稀KI溶液逐滴加入过量的稀AgNO3溶液中,得到AgI胶体II;
实验③:将提纯后的AgI胶体I与AgI胶体II进行混合,出现了黄色沉淀。
完成下列填空:
(3)写出制备AgI胶体I的离子方程式
(4)提纯AI胶体的方法如图所示。

材料X为
(5)本实验的探究结论是制备AgI胶体时反应物的用量对胶体粒子所带电性
22-23高一上·河北石家庄·期中
类题推荐
实验证明,胶体的凝聚能力主要取决于与胶粒带相反电荷的离子所带的电荷数,电荷数越大,凝聚能力越大。
(1)向Fe(OH)3胶体中加入下列电解质时,其凝聚能力最强的为_______
①NaCl ②FeCl3 ③K2SO4 ④Na3PO4
(2)为了把黏土溶胶(黏土胶体粒子带负电荷)变成较洁净的水,加入下列电解质时,_______(填字母)效果最明显。
(3)将少量FeCl3饱和溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:将FeCl3饱和溶液滴加到冷水中;
乙:将FeCl3饱和溶液滴加到NaOH溶液中;
丙:将FeCl3饱和溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
①丙中反应的化学方程式为_______ 。
②用最简单的方法判断丙中是否成功制备胶体,写出相关的操作、现象和结论_______ ,能产生该现象的原因是胶体粒子对光波的_______ 所致。
③向经过检验后的丙中逐滴加入稀盐酸,出现的现象为_______
④Fe(OH)3胶体能稳定存在的主要原因是_______ 。
⑤向丙中插入电极后通电,Fe(OH)3胶粒移向_______ (填“与电源负极相连”或“与电源正极相连”)的一极。
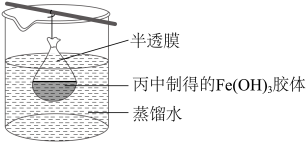
⑥可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。该方法名称为_______ 。设计实验证明该Fe(OH)3胶体中的杂质离子已经完全被除去:_______ 。
(1)向Fe(OH)3胶体中加入下列电解质时,其凝聚能力最强的为
①NaCl ②FeCl3 ③K2SO4 ④Na3PO4
(2)为了把黏土溶胶(黏土胶体粒子带负电荷)变成较洁净的水,加入下列电解质时,_______(填字母)效果最明显。
| A.BaCl2 | B.Al2(SO4)3 | C.KCl | D.CuSO4 |
甲:将FeCl3饱和溶液滴加到冷水中;
乙:将FeCl3饱和溶液滴加到NaOH溶液中;
丙:将FeCl3饱和溶液滴加到沸水中,继续加热煮沸得到红褐色透明液体。
①丙中反应的化学方程式为
②用最简单的方法判断丙中是否成功制备胶体,写出相关的操作、现象和结论
③向经过检验后的丙中逐滴加入稀盐酸,出现的现象为
④Fe(OH)3胶体能稳定存在的主要原因是
⑤向丙中插入电极后通电,Fe(OH)3胶粒移向
⑥可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。该方法名称为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网