解答题-结构与性质 适中0.65 引用1 组卷123
NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_______ 。
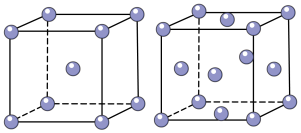
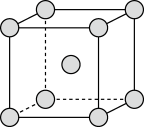
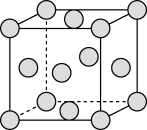
②实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
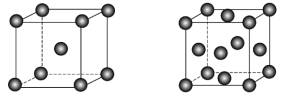
i.两种晶胞所含铁原子个数比为_______ 。
ii.图1晶胞的棱长为apm(1pm=1×10-10cm),则其密度ρ=_______ g·cm-3。
③我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是_______ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是_______ 。
②NaHCO3分解得Na2CO3, 空间结构为
空间结构为_______ 。
(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
①NH3BH3存在配位键,提供空轨道的是_______ 。
②比较熔点:NH3BH3_______ CH3CH3(填“>”或“<”)。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为
②实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:

i.两种晶胞所含铁原子个数比为
ii.图1晶胞的棱长为apm(1pm=1×10-10cm),则其密度ρ=
③我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是
②NaHCO3分解得Na2CO3,
(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
| 元素 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
①NH3BH3存在配位键,提供空轨道的是
②比较熔点:NH3BH3
22-23高三上·河南鹤壁·阶段练习
类题推荐
NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_______ ,N原子轨道表示式_______ 。
②实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:
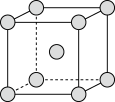
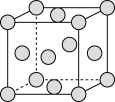
ⅰ.两种晶胞所含铁原子个数比为_______ 。
ⅱ.图1晶胞的棱长为a pm(1 pm = 1×10-10 cm),则其密度ρ =_______ g·cm﹣3.。
③我国科学家开发出Fe—LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是_______ 。
(2)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
①NH3的中心原子的杂化轨道类型为_______ 。
②NH3BH3存在配位键,提供空轨道的是_______ ,还有很多其他含氮配合物,如K2[Cu(CN)4]的配离子是_______ 、配合物[Cd(NH3)4](OH)2的配位体是_______ 。
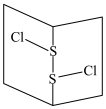
(3)常温下S2Cl2是橙黄色液体,其分子结构如图所示。少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。S2Cl2分子中含有_______ 键(填“极性”或“非极性”),是_______ 分子(填“极性”或“非极性”),S2Br2与S2Cl2分子结构相似,熔沸点S2Br2_______ S2Cl2(填“>”或“<”)。

(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为
②实际生产中采用铁的氧化物Fe2O3、FeO,使用前用H2和N2的混合气体将它们还原为具有活性的金属铁。铁的两种晶胞(所示图形为正方体)结构示意如下:


ⅰ.两种晶胞所含铁原子个数比为
ⅱ.图1晶胞的棱长为a pm(1 pm = 1×10-10 cm),则其密度ρ =
③我国科学家开发出Fe—LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是
(2)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
| 元素 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
①NH3的中心原子的杂化轨道类型为
②NH3BH3存在配位键,提供空轨道的是
(3)常温下S2Cl2是橙黄色液体,其分子结构如图所示。少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液。S2Cl2分子中含有

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网