解答题-工业流程题 适中0.65 引用1 组卷106
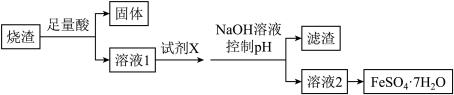
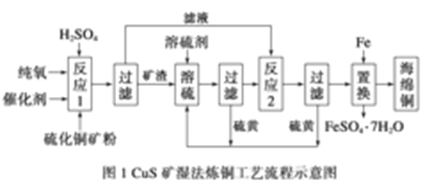
近年来,硫化铜矿(主要成分为CuFeS2和Cu2S)的湿法冶炼技术已经取得了很大的进展。现有一种催化氧化酸浸硫化铜矿的冶炼法,其工艺流程如图所示:
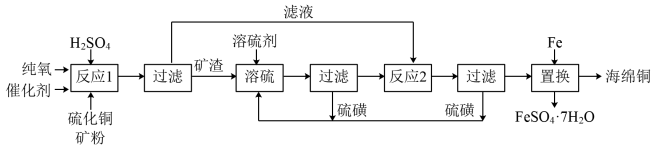
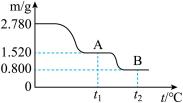
反应温度、固液比、反应时间和氯离子浓度都对铜的浸出率有较大的影响,下面是实验得出的这几种因素对铜的浸出率影响的变化曲线图(如图甲~丁所示)。
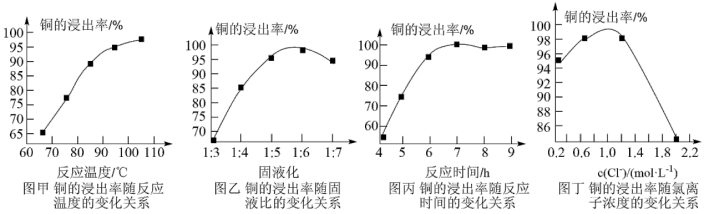
回答下列问题:
(1)铜的主要反应有:
反应Ⅰ:2CuFeS2+4O2 Cu2S+3SO2+2FeO(炉渣)
Cu2S+3SO2+2FeO(炉渣)
反应Ⅱ:2Cu2S+3O2 2Cu2O+2SO2
2Cu2O+2SO2
反应Ⅲ:_______
①反应Ⅰ、Ⅱ的两种含铜产物继续在1200℃条件下继续发生反应Ⅲ生成单质铜,该反应的氧化剂为_______
②由a mol CuFeS2生成a mol Cu,共消耗_______ mol O2(用含a表达式表示)。
(2)经查,硫黄、FeSO4·7H2O均可入药,用途广泛。湿法炼铜与火法炼铜相比,优点是_______ 、_______ (写出两点)。
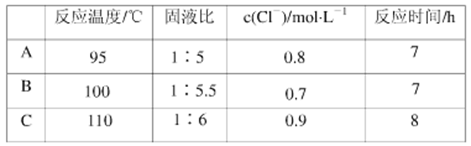
(3)根据实验以及工业生产的实际要求,从表中得出的最佳工艺条件为_______ (填字母)。
(4)副产品FeSO4·7H2O样品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取5.800g绿矾产品,经溶解、定容等步骤准确配制250mL溶液;
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中;
步骤3:用硫酸酸化的0.01000mol·L-1 KMnO4溶液滴定至终点,记录消耗KMnO4溶液体积;
步骤4:重复步骤2、步骤3一至两次。
①步骤2量取溶液所用仪器是_______ 。
②判断此滴定实验达到终点的方法是_______ 。
③数据处理:
计算上述样品中FeSO4·7H2O的质量分数为_______ (保留两位小数)。
④不考虑操作误差,用上述方法测定的样品中FeSO4·7H2O的质量分数偏低的原因可能是_______ 。

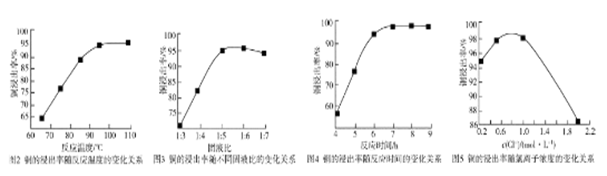
反应温度、固液比、反应时间和氯离子浓度都对铜的浸出率有较大的影响,下面是实验得出的这几种因素对铜的浸出率影响的变化曲线图(如图甲~丁所示)。

回答下列问题:
(1)铜的主要反应有:
反应Ⅰ:2CuFeS2+4O2
反应Ⅱ:2Cu2S+3O2
反应Ⅲ:_______
①反应Ⅰ、Ⅱ的两种含铜产物继续在1200℃条件下继续发生反应Ⅲ生成单质铜,该反应的氧化剂为
②由a mol CuFeS2生成a mol Cu,共消耗
(2)经查,硫黄、FeSO4·7H2O均可入药,用途广泛。湿法炼铜与火法炼铜相比,优点是
(3)根据实验以及工业生产的实际要求,从表中得出的最佳工艺条件为
| 选项 | 反应温度/℃ | 固液比 | c(Cl-)/(mol·L-1) | 反应时间/h |
| A | 95 | 1:5 | 0.8 | 7 |
| B | 100 | 1:5.5 | 0.7 | 7 |
| C | 110 | 1:6 | 0.9 | 8 |
(4)副产品FeSO4·7H2O样品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取5.800g绿矾产品,经溶解、定容等步骤准确配制250mL溶液;
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中;
步骤3:用硫酸酸化的0.01000mol·L-1 KMnO4溶液滴定至终点,记录消耗KMnO4溶液体积;
步骤4:重复步骤2、步骤3一至两次。
①步骤2量取溶液所用仪器是
②判断此滴定实验达到终点的方法是
③数据处理:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 40.01 |
| 2 | 25.00mL | 0.70 | 40.71 |
| 3 | 25.00mL | 0.20 | 39.20 |
计算上述样品中FeSO4·7H2O的质量分数为
④不考虑操作误差,用上述方法测定的样品中FeSO4·7H2O的质量分数偏低的原因可能是
22-23高三上·上海虹口·阶段练习
类题推荐
金属镓有“电子工业脊梁”的美誉,镓与铝的化学性质类似。从刚玉渣(含钛、镓的低硅铁合金,还含有少量氧化铝)回收镓的流程如图所示:

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
请回答下列问题:
(1)“酸浸”过程中为提高浸取率可采取的具体措施为______ 。(任写两条)
(2)“中和沉淀”过程中,滤液③的溶质主要成分为______ ,这一过程pH应调节的范围为______ 。
(3)“碱浸”过程中______ 用氨水代替NaOH溶液(选填“能”或“不能”)
(4)“碳酸化”过程中为防止镓损耗,不能通入过量 的原因为
的原因为______ (用离子方程式表示),由流程图可知酸性
______  。
。
(5)GaN具有优异的光电性能。工业上常采用在1100℃条件下,利用Ga与 反应可制备GaN,该过程的化学方程式为
反应可制备GaN,该过程的化学方程式为______ 。
(6)副产品 样品的纯度可用滴定法进行测定,实验步骤如下:
样品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取5.800g绿矾产品,经溶解、定容等步骤准确配制250mL溶液:
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中:
步骤3:用硫酸酸化的 溶液滴定至终点,记录消耗
溶液滴定至终点,记录消耗 溶液体积;
溶液体积;
步骤4:重复步骤2、步骤3一至两次。
①数据处理:
计算上述样品中 的质量分数为
的质量分数为______ (保留两位小数)。
②不考虑操作误差,用上述方法测定的样品中 的质量分数偏低的原因可能是
的质量分数偏低的原因可能是______ 。

溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 | ||||
| 开始沉淀时( | 4.5 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时( | 5.5 | 4.7 | 3.2 | 9.0 |
(1)“酸浸”过程中为提高浸取率可采取的具体措施为
(2)“中和沉淀”过程中,滤液③的溶质主要成分为
(3)“碱浸”过程中
(4)“碳酸化”过程中为防止镓损耗,不能通入过量
(5)GaN具有优异的光电性能。工业上常采用在1100℃条件下,利用Ga与
(6)副产品
步骤1:称取5.800g绿矾产品,经溶解、定容等步骤准确配制250mL溶液:
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中:
步骤3:用硫酸酸化的
步骤4:重复步骤2、步骤3一至两次。
①数据处理:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00mL | 0.02 | 40.01 |
| 2 | 25.00mL | 0.70 | 40.71 |
| 3 | 25.00mL | 0.20 | 39.20 |
②不考虑操作误差,用上述方法测定的样品中
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 Cu2S+3SO2+2FeO(炉渣); ②2Cu2S+3O2
Cu2S+3SO2+2FeO(炉渣); ②2Cu2S+3O2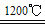 2Cu2O+2SO2;③2Cu2O+Cu2S
2Cu2O+2SO2;③2Cu2O+Cu2S