解答题-结构与性质 适中0.65 引用1 组卷114
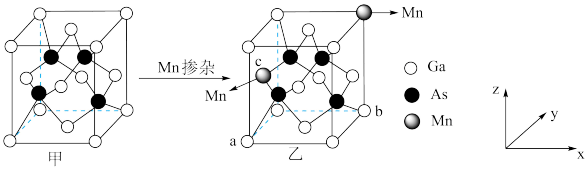
砷化镓( )是一种性能优良的半导体材料,工业上可通过如下的两个反应制取:
)是一种性能优良的半导体材料,工业上可通过如下的两个反应制取: 或
或 。
。
(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
(2) 的中心原子轨道杂化类型为
的中心原子轨道杂化类型为_______ , 中的三个碳原子和中心原子镓原子构成的空间构型是
中的三个碳原子和中心原子镓原子构成的空间构型是_______ ,写出一种与甲烷互为等电子体的离子的化学式:_______ 。
(3)上述反应涉及的几种元素中,电负性最大的元素是_______ ,砷可形成多种卤化物,其中 的沸点由低到高的原因为
的沸点由低到高的原因为_______ 。
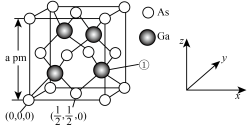
(4) 晶胞图及部分原子的分数坐标如下:
晶胞图及部分原子的分数坐标如下:
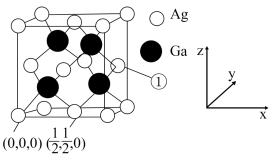
则①处原子的分数坐标为_______ ,已知紧邻的 原子之间的距离为
原子之间的距离为 ,紧邻的
,紧邻的 原子之间的距离为
原子之间的距离为 ,则
,则
_______ b,该晶胞的密度为_______  (用含a、阿伏加德罗常数
(用含a、阿伏加德罗常数 的式子表示)。
的式子表示)。
(1)基态砷原子的价层电子排布图为_______。氯元素的下列几种微粒中,若再失去一个电子,需要的能量最多的是_______(填标号)。
| A. | B. | C. | D. |
(3)上述反应涉及的几种元素中,电负性最大的元素是
(4)

则①处原子的分数坐标为
22-23高三上·江西吉安·阶段练习
类题推荐
碳元素形成的化合物种类繁多,应用广泛。回答下面问题:
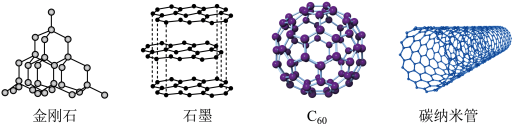
(1)如下图所示,是几种碳单质的空间模型。_______ (填化学式),石墨晶体属于_______ 晶体。属于共价晶体,且一个晶胞中含有8个碳原子的是_______ (填名称)。
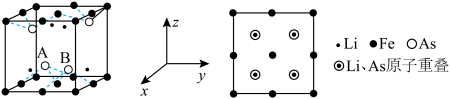
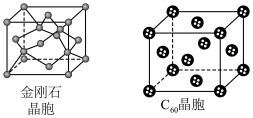
②金刚石和C60形成的晶胞模型如下图所示:
_______ 。
(2)由硅原子形成的三种微粒,电子排布式分别为:a.[Ne]3s23p2、b.[Ne]3s23p1、c.[Ne]3s23p14s1。
①三种微粒半径由大到小的顺序是_______ (用序号表示,下同。)
②再电离一个电子所需最低能量由大到小的顺序是_______ 。
(3)已知一些物质的熔点数据如下表:
①分析同族元素的氯化物SiCl4、GeCl4、SnCl4熔点变化趋势及其原因_______ 。
②SnCl4的熔点远低于NaCl的主要原因是_______ 。
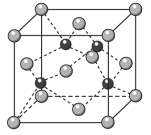
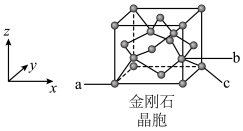
(4)已知金刚石晶胞结构如下图:_______ 。
②若金刚石的密度为d g/cm3,阿伏加德罗常数用 表示,则碳原子b和c之间的距离为
表示,则碳原子b和c之间的距离为_______ m(用含d和 的表达式表示,不用化简)。
的表达式表示,不用化简)。
(1)如下图所示,是几种碳单质的空间模型。
②金刚石和C60形成的晶胞模型如下图所示:
(2)由硅原子形成的三种微粒,电子排布式分别为:a.[Ne]3s23p2、b.[Ne]3s23p1、c.[Ne]3s23p14s1。
①三种微粒半径由大到小的顺序是
②再电离一个电子所需最低能量由大到小的顺序是
(3)已知一些物质的熔点数据如下表:
物质 | SiCl4 | GeCl4 | SnCl4 | NaCl |
熔点/℃ | -68.8 | -51.5 | -34.1 | 800.7 |
②SnCl4的熔点远低于NaCl的主要原因是
(4)已知金刚石晶胞结构如下图:
②若金刚石的密度为d g/cm3,阿伏加德罗常数用
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网