解答题-原理综合题 适中0.65 引用1 组卷72
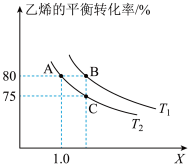
乙烯可用于制备乙醇:C2H4(g)+H2O(g) C2H5OH(g) ΔH1。向10L某恒容密闭容器中通入2 mol C2H4(g)和a mol H2O(g),发生上述反应,测得C2H4(g)的平衡转化率与投料比X[
C2H5OH(g) ΔH1。向10L某恒容密闭容器中通入2 mol C2H4(g)和a mol H2O(g),发生上述反应,测得C2H4(g)的平衡转化率与投料比X[ ]以及温度的关系如图所示。
]以及温度的关系如图所示。
(1)已知298K、101kPa下,2C2H5OH(l)=2C2H5OH(g) ΔH2=+83.0 kJ/mol,且C2H5OH(l)和C2H4(g)的燃烧热分别为1366.8 kJ/mol和1411.0 kJ/mol,则ΔH1=_______ 。
(2)反应从开始分别进行到A、B、C点时,放出或吸收的热量QA、QB、QC由大到小的顺序为_______ 。
(3)已知该反应的反应速率表达式为v正=k正·c(C2H4)·c(H2O),v逆=k逆·c(C2H5OH),其中k正、k逆为速率常数,只与温度有关。
①A、B点对应的该反应的平衡常数大小为:KA_______ KB(填“>”、“<”或“=”)。
②若A点对应的体系中,反应从开始到平衡所用时间是2min,则0~2min内H2O(g)的平均反应速率v(H2O)=_______ 。
③T2温度下, =
=_______ 。
④B点对应的体系中,a等于_______ ;A、B、C点对应体系的气体总压强pA、pB、pC由小到大的顺序为_______ 。(气体均看作理想气体)

(1)已知298K、101kPa下,2C2H5OH(l)=2C2H5OH(g) ΔH2=+83.0 kJ/mol,且C2H5OH(l)和C2H4(g)的燃烧热分别为1366.8 kJ/mol和1411.0 kJ/mol,则ΔH1=
(2)反应从开始分别进行到A、B、C点时,放出或吸收的热量QA、QB、QC由大到小的顺序为
(3)已知该反应的反应速率表达式为v正=k正·c(C2H4)·c(H2O),v逆=k逆·c(C2H5OH),其中k正、k逆为速率常数,只与温度有关。
①A、B点对应的该反应的平衡常数大小为:KA
②若A点对应的体系中,反应从开始到平衡所用时间是2min,则0~2min内H2O(g)的平均反应速率v(H2O)=
③T2温度下,
④B点对应的体系中,a等于
22-23高二上·辽宁朝阳·阶段练习
类题推荐
已知:
 。请回答下列问题:
。请回答下列问题:
(1)该反应在_______ (填“低温”、“高温”或“任何温度”下能自发进行。
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
(3)若在10 L的密闭容器内2 mol H2(g)与a molC2H4(g)进行上述反应,测得 的平衡转化率与投料比X,
的平衡转化率与投料比X, 以及温度的关系如图所示。
以及温度的关系如图所示。
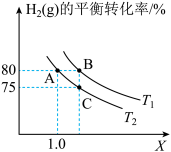
①反应从开始分别进行到A、B、C点时,_______ (填“吸收”或“放出”)的热量QA、QB、QC由大到小的顺序为_______ 。
②T1_______ (填“>”、“<”或“=”)T2。
③B点对应的体系中a=_______ 。A、B、C点对应体系的气体总压强pA、pB、pC由小到大的顺序为_______ 。
(4) ,
, ,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
,其中k正和k逆为速率常数,只与温度有关。若其他条件不变,则温度从T1变化到T2的过程中,下列推断合理的是_______(填标号)。
(1)该反应在
(2)若上述反应在恒温恒容密闭容器中进行,则下列条件能判断该反应达到平衡状态的是_______(填标号)。
| A.容器内混合气体的平均相对分子质量不变 | B.c正(H2)=c逆(C2H6) |
| C.容器内混合气体的压强不变 | D.容器内混合气体的密度不变 |

①反应从开始分别进行到A、B、C点时,
②T1
③B点对应的体系中a=
(4)
| A.k正增大的倍数大于k逆 | B.k正增大的倍数小于k逆 |
| C.k正减小的倍数大于 | D.k正减小的倍数小于k逆 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网