解答题-实验探究题 适中0.65 引用1 组卷232
氮是自然界各种生物体生命活动不可缺少的重要元素,氨元素的单质及化合物是中学化学中的重要物质。
(1)请回答下列问题:
① 的电子式为
的电子式为_______ 。
②下列说法涉及“氮的固定”的有_______ 。
A.谚语“雷雨发庄稼”
B.氨气遇到氯化氢时,生成氯化铵晶体
C.豆科植物的根瘤菌将氮气转化为氨
D.工业合成氨:
(2)某化学学习小组拟设计实验制取氨气并探究其有关性质,实验装置如下图。
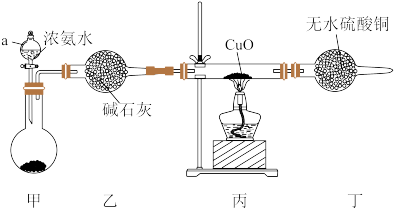
回答下列问题:
①仪器a的名称为_______ 。
②某同学提出该装置设计上有一定的缺陷,应在丁装置后添加一个盛有浓硫酸的洗气瓶,目的是_______ 。
③利用改进后的装置进行实验,一段时间后, 变为红色金属单质、无水
变为红色金属单质、无水 变蓝,同时生成一种无毒无污染的气体。根据上述信息写出
变蓝,同时生成一种无毒无污染的气体。根据上述信息写出 与
与 反应的化学方程式:
反应的化学方程式:_______ 。
④氨气可将有毒的 还原为氮气,该反应中氧化剂与还原剂的质量之比为
还原为氮气,该反应中氧化剂与还原剂的质量之比为_______ 。
(1)请回答下列问题:
①
②下列说法涉及“氮的固定”的有
A.谚语“雷雨发庄稼”
B.氨气遇到氯化氢时,生成氯化铵晶体
C.豆科植物的根瘤菌将氮气转化为氨
D.工业合成氨:
(2)某化学学习小组拟设计实验制取氨气并探究其有关性质,实验装置如下图。

回答下列问题:
①仪器a的名称为
②某同学提出该装置设计上有一定的缺陷,应在丁装置后添加一个盛有浓硫酸的洗气瓶,目的是
③利用改进后的装置进行实验,一段时间后,
④氨气可将有毒的
21-22高一下·贵州六盘水·期末
类题推荐
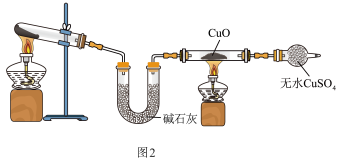
为测定氨分子中氮、氢原子个数比。某研究性学习小组设计了如下实验流程:

实验时,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的单质铜。
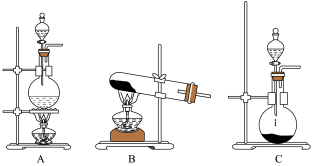
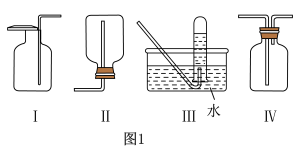
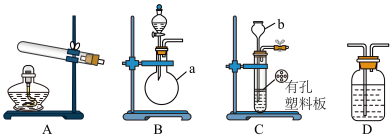
如图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
实验1测得反应前氧化铜的质量m1g、氧化铜反应后剩余固体的质量m2g、生成的氮气在标准状况下的体积V1L。
实验2测得洗气前装置D的质量m3g、洗气后装置D的质量m4g、生成的氮气在标准状况下的体积V2L。请回答下列问题:
(1)写出仪器a和b的名称分别是:圆底烧瓶和______________ 。
(2)检查A装置气密性的操作是_____________________________ 。
(3)实验1和实验2分别选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填或相关化学方程式写在下表的空格中。
(4)实验1用所测数据计算出氨分子中氮、氢的原子个数比为______________ 。(列式子,不计算结果)
(5)实验2用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是_____________________ 。为此,实验2在原有实验的基础上增加了一个装有某药品的实验仪器重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果。该药品和实验仪器的名称分别是__________ 和____________ 。

实验时,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装置,立即加热氧化铜。反应完成后,黑色的氧化铜转化为红色的单质铜。
如图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。

实验1测得反应前氧化铜的质量m1g、氧化铜反应后剩余固体的质量m2g、生成的氮气在标准状况下的体积V1L。
实验2测得洗气前装置D的质量m3g、洗气后装置D的质量m4g、生成的氮气在标准状况下的体积V2L。请回答下列问题:
(1)写出仪器a和b的名称分别是:圆底烧瓶和
(2)检查A装置气密性的操作是
(3)实验1和实验2分别选择了不同的方法制取氨气,请将实验装置的字母编号和制备原理填或相关化学方程式写在下表的空格中。
| 实验装置 | 实验药品 | 制备原理 | |
| 实验1 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为:① |
| 实验2 | ② | 浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用:③ |
(5)实验2用所测数据计算出氨分子中氮、氢的原子个数比明显小于理论值,其原因是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网