解答题-原理综合题 适中0.65 引用1 组卷122
Ⅰ、中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是高效、安全的杀菌消毒剂。
(1)漂白粉主要用于游泳池水等的杀菌和消毒,久置空气中会呈稀粥状而失去漂白作用,用化学方程式表示漂白粉在空气中失效的原因________________________________ 。84消毒液是一种家用消毒剂,不能用于钢制器具的消毒,原因是NaClO具有____ 性。
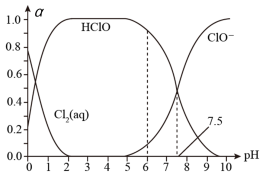
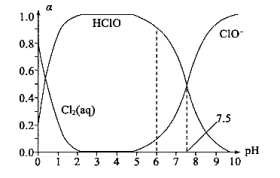
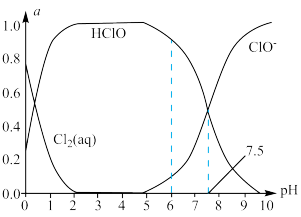
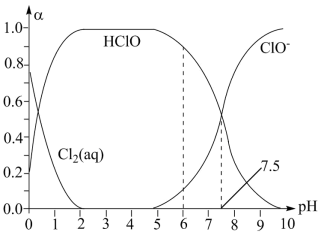
(2)新制氧水常用于杀菌消毒,在25°C时将氧气溶于水形成氯气-氯水体系。该体系中Cl2(aq)、HClO和ClO-的物质的量分数(a)能pH变化的关系如图所示。由图分析,用氯气处理饮用水时,pH=6 与pH=7.5两种情况下,pH=____ 时杀菌效果强。 当pH=7.5时,氯水中含氯元素的微粒有HClO、 ClO-和_______ 。
ClO2是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。
(3)根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为自来水的消毒剂。工业上常用NaClO3溶液和Na2SO3溶液混合并加入H2SO4酸化制得ClO2且产物中有Na2SO4,则在该反应中,氧化产物和还原产物的物质的量之比为______ 。
(4)已知C1O2在进行饮用水消毒时转化为Cl-,则ClO2与Cl2的消毒能力之比为______ (写最简整数比,消毒能力用单位质量清毒剂得电子多少来衡量)
Ⅱ、化学方法在文物保护中有重要作用,某博物馆修复出土铁器的部分过程如下:
(5)检测锈蚀产物主要成分的化学式为Fe3O4、Fe2O3 •H2O、FeO(OH)、 FeOCl,由产物可推测,铁器可能与____________________ (填2种反应物化学式)发生反应而被腐蚀。
分析认为,铁经过了如下腐蚀循环:
Ⅰ. Fe转化为Fe2+;
Ⅱ. Fe2+在自然环境中形成FeO(OH);
Ⅲ. FeO(OH)和 Fe2+反应形成致密的Fe3O4保护层;
Ⅳ. Fe3O4保护层转化为FeO(OH),如此往复腐蚀。
(6)FeOCl中铁的化合价为___ ;上述反应中是氧化还原反应的为_______ (填序号)。
(7)FeO(OH)和Fe2+反应的离子方程式为______________________ 。
(8)Ⅳ反应为Fe3O4+O2+H2O→FeO(OH),还原剂为________ ,每反应 1mol还原剂,转移电子_____ mol。
(1)漂白粉主要用于游泳池水等的杀菌和消毒,久置空气中会呈稀粥状而失去漂白作用,用化学方程式表示漂白粉在空气中失效的原因
(2)新制氧水常用于杀菌消毒,在25°C时将氧气溶于水形成氯气-氯水体系。该体系中Cl2(aq)、HClO和ClO-的物质的量分数(a)能pH变化的关系如图所示。由图分析,用氯气处理饮用水时,pH=6 与pH=7.5两种情况下,pH=

ClO2是国际上公认的安全、无毒、无“三致”效应(致癌、致畸、致突变)的杀菌消毒剂。
(3)根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为自来水的消毒剂。工业上常用NaClO3溶液和Na2SO3溶液混合并加入H2SO4酸化制得ClO2且产物中有Na2SO4,则在该反应中,氧化产物和还原产物的物质的量之比为
(4)已知C1O2在进行饮用水消毒时转化为Cl-,则ClO2与Cl2的消毒能力之比为
Ⅱ、化学方法在文物保护中有重要作用,某博物馆修复出土铁器的部分过程如下:
(5)检测锈蚀产物主要成分的化学式为Fe3O4、Fe2O3 •H2O、FeO(OH)、 FeOCl,由产物可推测,铁器可能与
分析认为,铁经过了如下腐蚀循环:
Ⅰ. Fe转化为Fe2+;
Ⅱ. Fe2+在自然环境中形成FeO(OH);
Ⅲ. FeO(OH)和 Fe2+反应形成致密的Fe3O4保护层;
Ⅳ. Fe3O4保护层转化为FeO(OH),如此往复腐蚀。
(6)FeOCl中铁的化合价为
(7)FeO(OH)和Fe2+反应的离子方程式为
(8)Ⅳ反应为Fe3O4+O2+H2O→FeO(OH),还原剂为
22-23高一上·山东威海·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网