解答题-实验探究题 0.4 引用1 组卷224
科学家舍勒和戴维对氯气的制取和研究做出了重大贡献。
Ⅰ.某化学小组设计如图装置制备少量纯净干燥的氯气,试回答下列问题:
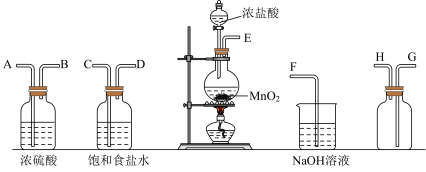
(1)盛有浓盐酸的仪器名称_______ ,装置的正确连接顺序为E→_______、_______→A、B→_______、_______→F。_______
(2)气体发生装置中发生反应的化学方程式为_______ 。
(3)装置中饱和食盐水的作用是_______ 。
(4)请用化学方程式表示装置中的氢氧化钠溶液的作用_______ 。
II.一种以氯气和生石灰(CaO)为原料制备KClO3的流程如下:
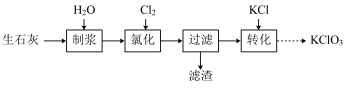
注:氯化过程中Cl2与Ca(OH)2作用生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2。
(5)氯化过程中须缓慢通入Cl2,缓慢通入的目的是_______ 。
(6)根据如图的溶解度曲线,回答下列问题。

向滤液中加入过量KCl固体可将溶液中Ca(ClO3)2转化为KClO3固体而析出的原因是_______ 。若溶液中KClO3的含量为100g∙L−1,从该溶液中尽可能多地析出KClO3固体的方法是_______ 。
Ⅰ.某化学小组设计如图装置制备少量纯净干燥的氯气,试回答下列问题:

(1)盛有浓盐酸的仪器名称
(2)气体发生装置中发生反应的化学方程式为
(3)装置中饱和食盐水的作用是
(4)请用化学方程式表示装置中的氢氧化钠溶液的作用
II.一种以氯气和生石灰(CaO)为原料制备KClO3的流程如下:

注:氯化过程中Cl2与Ca(OH)2作用生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2。
(5)氯化过程中须缓慢通入Cl2,缓慢通入的目的是
(6)根据如图的溶解度曲线,回答下列问题。

向滤液中加入过量KCl固体可将溶液中Ca(ClO3)2转化为KClO3固体而析出的原因是
22-23高一上·福建莆田·期中


