解答题-原理综合题 适中0.65 引用1 组卷74
由化学能产生热能是目前人类使用能源的主要途径。回答下列问题:
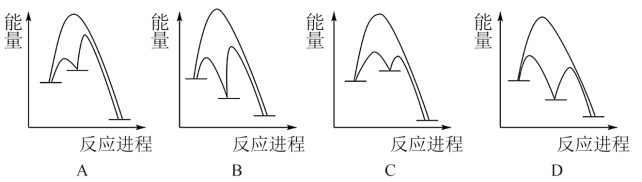
(1)图1表示反应 的能量变化。
的能量变化。
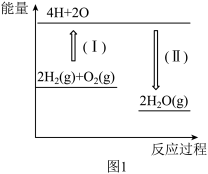
已知断开1molH-H键、1molO=O键和1molH-O键分别需要消耗436kJ、496kJ和460kJ的能量。则反应过程(II)中生成2mol (g)时
(g)时_______ (填“吸收”或“放出”)_______ kJ能量。
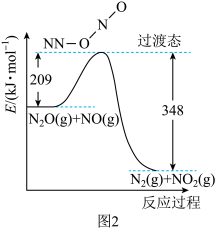
(2)由 和NO反应生成
和NO反应生成 和
和 的能量变化如图2所示。其正反应的活化能为
的能量变化如图2所示。其正反应的活化能为_______  ,若反应生成
,若反应生成 ,其
,其
_______  。
。
(3)已知某温度时,反应I:
 ;
;
反应II:
 。
。
CO(g)与 (s)反应生成
(s)反应生成 (s),该反应的热化学方程式为
(s),该反应的热化学方程式为_______ 。
(4)I.
II.
反应 的
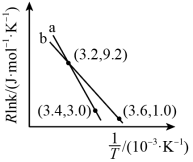
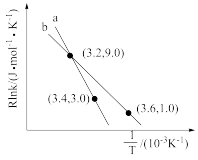
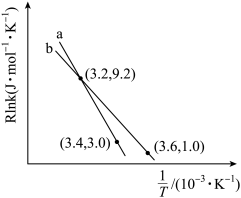
的 经验公式的实验数据如图中曲线
经验公式的实验数据如图中曲线 所示,已知
所示,已知 经验公式为
经验公式为 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数
为常数 。则该反应的活化能Ea=
。则该反应的活化能Ea=______ kJ/mol。当改变外界条件时,实验数据如图中的曲线 所示,则实验可能改变的外界条件是
所示,则实验可能改变的外界条件是_______ 。
(1)图1表示反应

已知断开1molH-H键、1molO=O键和1molH-O键分别需要消耗436kJ、496kJ和460kJ的能量。则反应过程(II)中生成2mol
(2)由

(3)已知某温度时,反应I:
反应II:
CO(g)与
(4)I.
II.
反应

22-23高二上·新疆省直辖县级单位·阶段练习
类题推荐
I.某合成气的主要成分是一氧化碳和氢气,可用于合成甲醚等清洁燃料。由天然气获得该合成气过程中可能发生的反应有
①CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
②CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。_______ ;10 min时,改变的外界条件可能是_______ 。
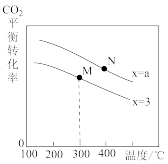
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象_______ 。
(3)上述生成Ni(CO)4(g)的反应为_______ 反应(填“放热”或“吸热”)
(4)在25℃时,反应Ni(CO)4(g)⇌Ni(s)+4CO(g)的平衡常数为_______ 。
(5)在80℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v正_______ v逆。
(6)在80℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为_______ 。
①CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+206.1 kJ·mol-1
②CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH2=+247.3 kJ·mol-1
③CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示。

(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等。在相同温度下发生反应②,并维持反应过程中温度不变。已知甲容器中CH4的转化率随时间的变化如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象

| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
(4)在25℃时,反应Ni(CO)4(g)⇌Ni(s)+4CO(g)的平衡常数为
(5)在80℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol·L-1,则此时v正
(6)在80℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网