解答题-实验探究题 较难0.4 引用1 组卷359
项目小组制备草酸 并测量其纯度。实验室制备草酸的流程如下:
并测量其纯度。实验室制备草酸的流程如下:

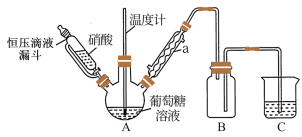
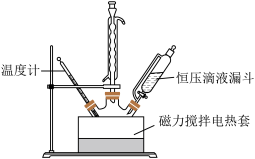
(1)草酸的制备。草酸制备的主要装置如图所示。
①将100mL淀粉水乳液和少许浓硫酸混合,加入三颈瓶中,搅拌,控温85-90℃,反应40分钟,使淀粉充分水解成葡萄糖 。检验淀粉已经水解完全的方法是
。检验淀粉已经水解完全的方法是_______ 。
②将质量比为2∶1.5∶0.0002的浓硝酸、浓硫酸和钒触媒的混合液加入恒压滴液漏斗中,分批加入到烧瓶内的水解液中,控温60℃,搅拌,反应3h左右。实验中若混酸滴加过快,将会导致草酸产率下降。可能的原因是_______ 。
③实验中,冷凝管可使尾气排出。冷凝管的主要作用还有_______ 。为防止污染,从冷凝管上部排出的气体可采取的处理方法是_______ 。
(2)产品纯度测定。称取上述得到的粗产品9.00g,配成1000mL溶液,取5.00mL溶液放入锥形瓶中,再稀释到20mL,用 酸性
酸性 标准溶液滴定至恰好反应完全,消耗
标准溶液滴定至恰好反应完全,消耗 溶液18.00mL。
溶液18.00mL。
已知:测定过程中发生的反应为
①滴定过程中的操作是_______ 。
②草酸产品的纯度为_______ (产品中的杂质不参与反应,写出计算过程)。

(1)草酸的制备。草酸制备的主要装置如图所示。

①将100mL淀粉水乳液和少许浓硫酸混合,加入三颈瓶中,搅拌,控温85-90℃,反应40分钟,使淀粉充分水解成葡萄糖
②将质量比为2∶1.5∶0.0002的浓硝酸、浓硫酸和钒触媒的混合液加入恒压滴液漏斗中,分批加入到烧瓶内的水解液中,控温60℃,搅拌,反应3h左右。实验中若混酸滴加过快,将会导致草酸产率下降。可能的原因是
③实验中,冷凝管可使尾气排出。冷凝管的主要作用还有
(2)产品纯度测定。称取上述得到的粗产品9.00g,配成1000mL溶液,取5.00mL溶液放入锥形瓶中,再稀释到20mL,用
已知:测定过程中发生的反应为
①滴定过程中的操作是
②草酸产品的纯度为
22-23高三上·江苏无锡·期中
类题推荐
某实验小组利用硫渣(主要成分为Sn,含少量 、
、 、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:
、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知: 遇水极易水解。
遇水极易水解。

相关产物的熔沸点:
(1)冷凝管的出水口为___________ (填“m”或“n”),装有碱石灰的仪器名称为___________ 。
(2)A中发生反应的化学方程式___________ 。
(3)下列有关操作的说法错误的是___________ 。
a.先点燃酒精灯,待硫渣熔化后,打开分液漏斗的活塞,并控制适当流速
b.若无装置C,会导致产物 产率降低
产率降低
c.碱石灰的主要作用是吸收多余的氯气和防止空气中的水蒸气影响 制备
制备
(4) 极易水解产生
极易水解产生 溶胶,写出
溶胶,写出 水解的化学方程式
水解的化学方程式___________ 。
(5)实验结束后,将三颈烧瓶中得到的物质冷却至室温,过滤得到液态粗产品,粗产品再___________ (填操作名称)可得到纯净的 。
。
(6)用碘量法测量产品的纯度:取10.00g产品溶于水,加入 标准
标准 溶液20.00mL,并加入少量的淀粉溶液,用
溶液20.00mL,并加入少量的淀粉溶液,用 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①
②
③
则滴定终点时锥形瓶内溶液的颜色变化___________ ,产品中 的质量分数
的质量分数___________ (保留四位有效数字)。

相关产物的熔沸点:
| 物质性质 | S | CuCl | ||||
| 熔点/℃ | -18 | 112 | -33 | 246 | 426 | 501 |
| 沸点/℃ | 130 | 444 | 114 | 652 | 1490 | 951 |
(1)冷凝管的出水口为
(2)A中发生反应的化学方程式
(3)下列有关操作的说法错误的是
a.先点燃酒精灯,待硫渣熔化后,打开分液漏斗的活塞,并控制适当流速
b.若无装置C,会导致产物
c.碱石灰的主要作用是吸收多余的氯气和防止空气中的水蒸气影响
(4)
(5)实验结束后,将三颈烧瓶中得到的物质冷却至室温,过滤得到液态粗产品,粗产品再
(6)用碘量法测量产品的纯度:取10.00g产品溶于水,加入
①
②
③
则滴定终点时锥形瓶内溶液的颜色变化
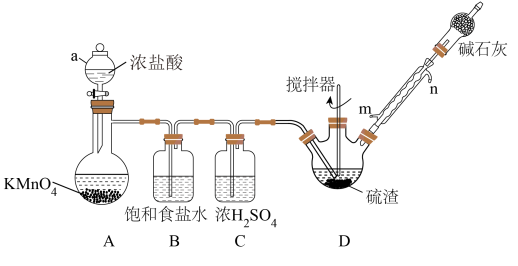
某实验小组利用硫渣(主要成分为Sn,含少量Cu2S、Pb、As等)与氯气反应制备四氯化锡,其过程如图所示(夹持、加热及控温装置略)。已知:SnCl4遇水极易水解。
相关产物的熔沸点:
(1)仪器a的名称___________ ,A中发生反应的化学方程式___________ 。
(2)冷凝管的进水口为___________ (填“m”或“n”),碱石灰的作用为___________ 。
(3)如果缺少B装置,可能造成的影响为___________ 。
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,___________ (填操作名称,下同),得到粗产品,粗产品再___________ 可得到纯净的SnCl4。
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用 的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
的硫代硫酸钠标准溶液滴定过量的碘。滴定终点时消耗20.00mL硫代硫酸钠标准溶液。测定过程中发生的相关反应:
①
②
③
则产品中SnCl4的质量分数___________ (保留三位有效数字)。某同学认为粗产品中会溶有少量氯气,导致测量结果___________ (填“偏高”“偏低”或“无影响”)。

相关产物的熔沸点:
| 物质性质 | SnCl4 | SnCl2 | CuCl | PbCl2 | AsCl3 | S |
| 熔点/℃ | -33 | 246 | 426 | 501 | -18 | 112 |
| 沸点/℃ | 114 | 652 | 1490 | 951 | 130 | 444 |
(2)冷凝管的进水口为
(3)如果缺少B装置,可能造成的影响为
(4)实验结束后,将三颈烧瓶中得到的物质冷却至室温,
(5)用碘量法测量粗产品的纯度:取10.00g粗产品溶于水,加入0.100mol·L-1标准I2溶液20.00mL,并加入少量的淀粉溶液:用
①
②
③
则产品中SnCl4的质量分数
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网