解答题-工业流程题 适中0.65 引用2 组卷191
氢氧化镍[Ni(OH)2]常用于制备金属镍及镍的重要化合物。一种用铁镍合金废料(还含有少量铜、钙、镁、硅的氧化物)制备纯度较高氢氧化镍的工艺流程如图:
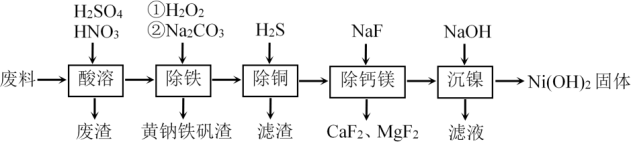
已知:H2S的电离常数K1=1.3×10-7,K2=7.1×10-15;Ksp[CuS]=6.0×10-36;Ksp[Ni(OH)2]=1.0×10-15.6。
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,还原产物为N2,金属镍溶解的离子方程式是_____ 。
(2)“除铁”加入Na2CO3时,生成黄钠铁矾(NaFe3(SO4)2(OH)6)的离子方程式是____ ;“除铁”时,将“铁”转化成颗粒较大的黄钠铁矾沉淀对后续操作较为有利,原因是____ 。
(3)“除铜”时,反应的离子方程式为H2S+Cu2+=CuS+2H+,该反应平衡常数K=____ 。
(4)“除钙镁”过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是_____ 。
(5)“沉镍”前c(Ni2+)=1.0mol/L,加入少量浓NaOH溶液,若忽略加入浓NaOH溶液对溶液体积的影响,则开始沉淀时溶液的pH=____ 。

已知:H2S的电离常数K1=1.3×10-7,K2=7.1×10-15;Ksp[CuS]=6.0×10-36;Ksp[Ni(OH)2]=1.0×10-15.6。
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,还原产物为N2,金属镍溶解的离子方程式是
(2)“除铁”加入Na2CO3时,生成黄钠铁矾(NaFe3(SO4)2(OH)6)的离子方程式是
(3)“除铜”时,反应的离子方程式为H2S+Cu2+=CuS+2H+,该反应平衡常数K=
(4)“除钙镁”过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是
(5)“沉镍”前c(Ni2+)=1.0mol/L,加入少量浓NaOH溶液,若忽略加入浓NaOH溶液对溶液体积的影响,则开始沉淀时溶液的pH=
22-23高三上·福建莆田·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网