解答题-工业流程题 较难0.4 引用2 组卷267
《中国锰业》一文提出用废铁屑还原软锰矿,制取高纯硫酸锰的工艺流程如下图所示。某公司提供的软锰矿,其主要成分是二氧化锰,其中还含有少量Fe、CaO、MgO、 及重金属等。
及重金属等。
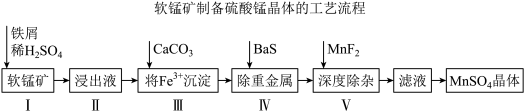
(1)I中加铁屑而不加铁块的原因是_______ 。
(2)写出I中铁屑与软锰矿发生的主要反应的离子方程式_______ 。
(3)加 之前需要加双氧水的作用
之前需要加双氧水的作用_______ ,结合下表说明,加 控制溶液pH的范围是
控制溶液pH的范围是_______ 。
可能用到的数据如下,不同金属离子沉淀的pH
已知: ,
,
(4)深度除杂中加入 的作用是除去钙离子、镁离子,用平衡移动原理解释
的作用是除去钙离子、镁离子,用平衡移动原理解释_______ 。
(5)从滤液中获取 晶体的方法是
晶体的方法是_______ 、趁热过滤。
硫酸锰在不同温度下的溶解度表
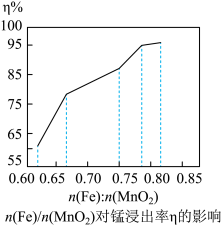
(6)为探究稀硫酸介质中湿法还原软锰矿制备硫酸锰的最佳工艺条件,研究了 对锰浸出率η的影响。如图实验条件为
对锰浸出率η的影响。如图实验条件为 ,反应温度为50℃,反应时间为80min。请结合图像分析
,反应温度为50℃,反应时间为80min。请结合图像分析 约为
约为_______ 最合适,并说出理由_______ 。

(1)I中加铁屑而不加铁块的原因是
(2)写出I中铁屑与软锰矿发生的主要反应的离子方程式
(3)加
可能用到的数据如下,不同金属离子沉淀的pH
| 氢氧化物 | |||
| 开始沉淀pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全pH | 3.7 | 9.7 | 9.8 |
(4)深度除杂中加入
(5)从滤液中获取
硫酸锰在不同温度下的溶解度表
| 温度/℃ | 50 | 80 | 90 | 100 |
| 溶解度l(/100g水) | 58 | 48 | 42 | 34 |

22-23高二上·北京西城·期中
类题推荐
中国锰业》一文提出用废铁屑还原软锰矿,制取高纯硫酸锰的工艺流程如图所示。软锰矿,其主要成分是二氧化锰,其中还含有少量Fe、CaO、MgO、SiO2及重金属等。

(1)I中加铁屑而不加铁块的原因是___________ 。
(2)步骤I中加入铁屑的作用是___________ ,I中若用H2C2O4(草酸)代替铁屑,写出发生反应的化学方程式为___________ 。
(3)步骤Ⅲ中,加CaCO3之前需要加双氧水的作用是___________ ,结合下表说明,加CaCO3控制溶液pH的范围是___________ 。
可能用到的数据如下:不同金属离子沉淀的pH
(4)硫酸锰晶体(MnSO4·H2O)在1150℃高温下易分解,产物是Mn3O4、含硫化合物、水,在该条件下硫酸锰晶体分解反应的化学方程式是___________ 。
(5)请根据下表分析,从滤液中获取MnSO4晶体的方法是___________ 。硫酸锰在不同温度下的溶解度表

(1)I中加铁屑而不加铁块的原因是
(2)步骤I中加入铁屑的作用是
(3)步骤Ⅲ中,加CaCO3之前需要加双氧水的作用是
可能用到的数据如下:不同金属离子沉淀的pH
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全pH | 3.7 | 9.7 | 9.8 |
(5)请根据下表分析,从滤液中获取MnSO4晶体的方法是
| 温度/℃ | 50 | 80 | 90 | 100 |
| 溶解度(g/100g水) | 58 | 48 | 42 | 34 |
软锰矿(成分如表1所示)的成分是二氧化锰,其中还含有少量二氧化硅、铁、氧化铝以及少量的重金属等。废铁屑还原软锰矿生产高纯硫酸锰晶体的工艺流程如图1所示。
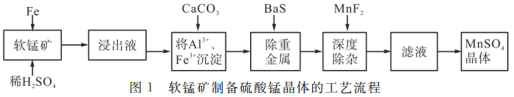
表1软锰矿的化学成分
(1)浸出液中检测到存在Fe3+,软锰矿与铁屑发生的离子反应是___________ ;
(2)加入碳酸钙之前需要加入双氧水的作用是___________ ,用碳酸钙除去铁、铝的原理是___________ 。(表2数据可供参考)。
表2不同金属离子沉淀的pH
(3)深度除杂中所加二氟化锰的作用是___________ 。
(4)从滤液中获得硫酸锰晶体的方法是___________ 。(硫酸锰在不同温度下的溶解度见表3)
表3硫酸锰在不同温度下的溶解度
(5)H2SO4/MnO2的物质的量比不同对锰的浸出率η有影响;实验表明,当H2SO4、MnO2的物质的量比2.1∶1锰的浸出率较高(见图2),请结合反应原理说明原因:___________ 。
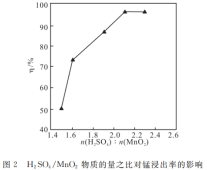

表1软锰矿的化学成分
| 成分 | 含量/% | 成分 | 含量/% |
| MnO2 | 35.23 | Fe | 2.16 |
| SiO2 | 15.67 | Al2O3 | 3.34 |
| MgO | 0.18 | CaO | 4.82 |
(2)加入碳酸钙之前需要加入双氧水的作用是
表2不同金属离子沉淀的pH
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 1.5 | 6.5 | 3.3 | 7.7 |
| 沉淀完全 | 3.7 | 9.7 | 5.2 | 9.8 |
(4)从滤液中获得硫酸锰晶体的方法是
表3硫酸锰在不同温度下的溶解度
| 温度/℃ | 50 | 80 | 90 | 100 |
| 溶解度/(g/100g水) | 58 | 48 | 42 | 34 |

工业上可用软锰矿制备硫酸锰。某生产硫酸锰的工艺流程如下:
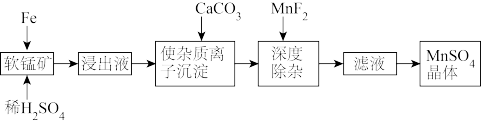
已知:①软锰矿的主要成分是MnO2,还含有SiO2、CaO、 Al2O3、 Fe2O3等。
②MnO2在酸性条件下氧化性较强。
③不同金属离子沉淀的pH
④MnSO4在不同温度下的溶解度
完成下列填空:
(1)软锰矿与铁、稀硫酸可能发生的氧化还原反应有:Fe+2H+→Fe2++H2↑、_______ 、_______ 。(再写两个离子反应方程式)
(2)浸出液中含Fe2+和Fe3+。写出检验浸出液中含Fe2+的方法。_______ 。
(3)加入CaCO3之前需加入H2O2,选H2O2的理由是:_______ 。
(4)加入MnF2的目的可能是:_______ 。
(5)从滤液中获得MnSO4晶体的方法是:_______ 。
(6)在n(H2SO4):n(MnO2)=2.1:1、反应温度为50℃条件下,探究n(Fe):n(MnO2)对锰浸出率的影响,实验数据如图所示。工业上宜选择n(Fe):n(MnO2)=0.78:1,请结合图象说明原因。_______ 。


已知:①软锰矿的主要成分是MnO2,还含有SiO2、CaO、 Al2O3、 Fe2O3等。
②MnO2在酸性条件下氧化性较强。
| 物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 1.9 | 6.5 | 3.3 | 7.7 |
| 沉淀完全 | 3.7 | 9.7 | 5.2 | 9.8 |
④MnSO4在不同温度下的溶解度
| 温度/°C | 50 | 80 | 90 | 100 |
| 溶解度/(g/100g水) | 58 | 48 | 42 | 34 |
(1)软锰矿与铁、稀硫酸可能发生的氧化还原反应有:Fe+2H+→Fe2++H2↑、
(2)浸出液中含Fe2+和Fe3+。写出检验浸出液中含Fe2+的方法。
(3)加入CaCO3之前需加入H2O2,选H2O2的理由是:
(4)加入MnF2的目的可能是:
(5)从滤液中获得MnSO4晶体的方法是:
(6)在n(H2SO4):n(MnO2)=2.1:1、反应温度为50℃条件下,探究n(Fe):n(MnO2)对锰浸出率的影响,实验数据如图所示。工业上宜选择n(Fe):n(MnO2)=0.78:1,请结合图象说明原因。

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


