解答题-原理综合题 适中0.65 引用1 组卷57
合成氨工业涉及固体燃料的气化,需要研究 与
与 之间的转化。为了弄清其规律,让一定量的
之间的转化。为了弄清其规律,让一定量的 与足量碳在体积可变的密闭容器中反应:
与足量碳在体积可变的密闭容器中反应:
 ,测得压强、温度对
,测得压强、温度对 、
、 的平衡组成的影响如图所示,回答下列问题:
的平衡组成的影响如图所示,回答下列问题:
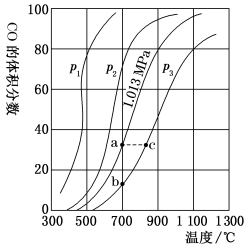
(1) 、
、 、
、 的大小关系是
的大小关系是_______ ,欲提高C与CO2反应中CO2的平衡转化率,应采取的措施为_______ 。图中a、b、c三点对应的平衡常数大小关系是_______ 。
(2)一定条件下,在 与足量碳反应所得平衡体系中加入
与足量碳反应所得平衡体系中加入 和适当催化剂,有下列反应发生:
和适当催化剂,有下列反应发生:
反应1:

反应2:

①则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是_______ 。
②已知 时相关化学键键能数据为:
时相关化学键键能数据为:
根据键能计算,
_______ 。

(1)
(2)一定条件下,在
反应1:
反应2:
①则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是
②已知
| 化学键 | H-H | O-H | C-H | C≡O |
| 436 | 465 | 413 | 1076 |
根据键能计算,
22-23高二上·山东临沂·阶段练习
类题推荐
合成氨工业涉及固体燃料的气化,需要研究CO2与CO之间的转化。为了弄清其规律,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)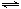 2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
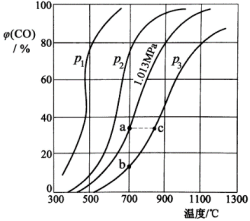
回答下列问题:
(1)p1、p2、p3的大小关系是______________ ,图中a、b、c三点对应的平衡常数大小关系是______________________ 。
(2)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:
反应1:CO(g)+3H2(g)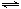 CH4(g)+H2O(g) ∆H1= a kJ/mol
CH4(g)+H2O(g) ∆H1= a kJ/mol
反应2:CO(g)+H2O(g)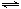 CO2(g)+H2(g) ∆H2= b kJ/mol
CO2(g)+H2(g) ∆H2= b kJ/mol
① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是_________________________ 。
② 已知298 K时相关化学键键能数据为:
则根据键能计算,∆H1=________________ 。反应1自发的条件是_____________ 。(填“较高温度”、“较低温度”、“任意温度”)
(3)一定条件下,CO2(g)+3H2(g)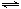 CH3OH(g)+H2O(g) ΔH3,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K值=
CH3OH(g)+H2O(g) ΔH3,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K值=_____________ (用分数表示),若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡时CH3OH的转化率为_____________ ,若平衡后再充入4 mol的N2,则c(CO2)和原平衡比较是___________ 。(填“增大”、“减小”、“不变”)
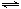 2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
回答下列问题:
(1)p1、p2、p3的大小关系是
(2)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:
反应1:CO(g)+3H2(g)
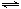 CH4(g)+H2O(g) ∆H1= a kJ/mol
CH4(g)+H2O(g) ∆H1= a kJ/mol反应2:CO(g)+H2O(g)
 CO2(g)+H2(g) ∆H2= b kJ/mol
CO2(g)+H2(g) ∆H2= b kJ/mol① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是
② 已知298 K时相关化学键键能数据为:
| 化学键 | H—H | O—H | C—H |  |
| E/(kJ·mol-1) | 436 | 465 | 413 | 1076 |
则根据键能计算,∆H1=
(3)一定条件下,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH3,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K值=
CH3OH(g)+H2O(g) ΔH3,向体积为2 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K值= 合成氨工业涉及固体燃料的气化,需要研究CO2与CO之间的转化。为了弄清其规律,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)  2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示,回答下列问题:
2CO(g) ∆H,测得压强、温度对CO、CO2的平衡组成的影响如图所示,回答下列问题:
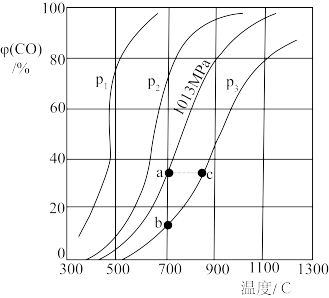
(1)p1、p2、p3的大小关系是________ ,图中a、b、c三点对应的平衡常数大小关系是______________________ 。
(2)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:反应1:CO(g)+3H2(g) CH4(g)+H2O(g) ∆H1= a kJ/mol
CH4(g)+H2O(g) ∆H1= a kJ/mol
反应2:CO(g)+H2O(g) CO2(g)+H2(g) ∆H2= b kJ/mol
CO2(g)+H2(g) ∆H2= b kJ/mol
① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是____________ 。
② 已知298 K时相关化学键键能数据为:
则根据键能计算,∆H1=________________ 。反应1自发进行的条件是___________ 。(填“较高温度”、“较低温度”、“任意温度”)
(3)一定条件下,CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH3,向固定容积为1 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K =
CH3OH(g)+H2O(g) ΔH3,向固定容积为1 L的密闭容器中充入2 mol CO2和6 mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数K =_________ (用分数表示);若开始时充入2 mol CH3OH(g) 和2 mol H2O(g)达到相同平衡状态时,CH3OH的转化率为_______ ;若平衡后再充入4 mol的N2,则c(CO2)和原平衡比较是_________ 。(填“增大”、“减小”、“不变”)
(4)如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
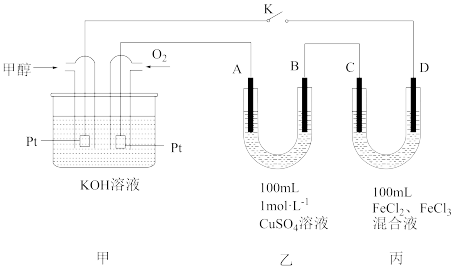
①甲中负极的电极反应式为_______________ ,丙中C极的电极反应式为___________ 。
② 乙中A极析出的气体在标准状况下的体积为__________________ 。

(1)p1、p2、p3的大小关系是
(2)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:反应1:CO(g)+3H2(g)
反应2:CO(g)+H2O(g)
① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是
② 已知298 K时相关化学键键能数据为:
| 化学键 | H—H | O—H | C—H | |
| E/(kJ·mol-1) | 436 | 465 | 413 | 1076 |
则根据键能计算,∆H1=
(3)一定条件下,CO2(g)+3H2(g)
(4)如图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。

①甲中负极的电极反应式为
② 乙中A极析出的气体在标准状况下的体积为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



