解答题-工业流程题 适中0.65 引用3 组卷231
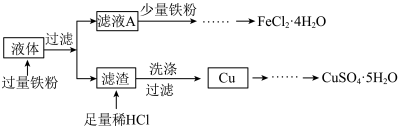
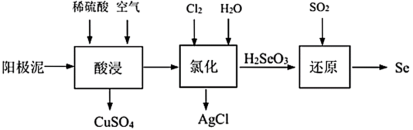
某粗铜精炼得到的阳极泥主要成分为Cu、Se、Ag2Se等,从中提取Se的工艺流程如下:
(1)“酸浸”过程中,加入稀硫酸并通入空气的目的是_______ 。
(2)“氯化”过程中发生如下转化:
①Se转化为H2SeO3,反应方程式为_______ 。
②Ag2Se转化为AgCl,结合化学用语从化学平衡的角度解释原因_______ 。
(3)“还原”过程中发生反应的化学方程式为_______ 。
(4)滴定法测定“酸浸”过程所得CuSO4溶液的浓度,其基本原理为:
第一步:
第二步:
①由反应原理可知滴定所用的指示剂为_______ 。
②若CuSO4溶液体积为25mL,滴定至终点时消耗c mol/L Na2S2O3溶液V mL,则CuSO4溶液的物质的量浓度为_______ mo/L。
③若第一步使用的KI溶液过量,对滴定结果的影响是_______ (填“偏大”或“偏小”或“不影响”)。
| 化学式 | Ag2Se | AgCl |
| Ksp(常温) |
(2)“氯化”过程中发生如下转化:
①Se转化为H2SeO3,反应方程式为
②Ag2Se转化为AgCl,结合化学用语从化学平衡的角度解释原因
(3)“还原”过程中发生反应的化学方程式为
(4)滴定法测定“酸浸”过程所得CuSO4溶液的浓度,其基本原理为:
第一步:
第二步:
①由反应原理可知滴定所用的指示剂为
②若CuSO4溶液体积为25mL,滴定至终点时消耗c mol/L Na2S2O3溶液V mL,则CuSO4溶液的物质的量浓度为
③若第一步使用的KI溶液过量,对滴定结果的影响是
22-23高二上·北京海淀·期中
类题推荐
工业上用含三价钒(V2O3)为主的某石煤为原料(含有Al2O3、CaO等杂质),钙化法焙烧制备V2O5,其流程如下:

【资料】+5价钒在溶液中的主要存在形式与溶液pH 的关系:
(1)焙烧:向石煤中加生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式是_______________________ 。
(2)酸浸:
①Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的pH=4,Ca(VO3)2溶于盐酸 的离子方程式是__________ 。
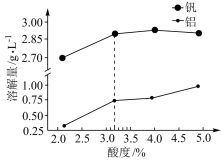
②酸度对钒和铝的溶解量的影响如下图所示: 酸浸时溶液的酸度控制在大约3.2%,根据右图推测,酸浸时不选择更高酸度的原因是_________________ 。
(3)转沉:将浸出液中的钒转化为NH4VO3固体,其流程如下:
①浸出液中加入石灰乳的作用是________________________ 。
②已知CaCO3的溶解度小于Ca3(VO4)2。向Ca3(VO4)2沉淀中加入(NH4)2CO3溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:______________ 。
③向(NH4)3VO4溶液中加入NH4Cl溶液,控制溶液的pH=7.5。当pH>8时,NH4VO3的产量明显降低,原因是_________________________________________ 。
(4)测定产品中V2O5的纯度:称取ag产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1mL c1mol·L−1(NH4)2Fe(SO4)2溶液(VO2++2H++Fe2+=VO2++Fe3++H2O)。最后用c2mol·L−1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO4−被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是______ 。(V2O5的摩尔质量:182 g·mol−1)

【资料】+5价钒在溶液中的主要存在形式与溶液pH 的关系:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 | VO2+ | VO3− | V2O74− | VO43− |
(2)酸浸:
①Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的pH=4,Ca(VO3)2溶于盐酸 的离子方程式是
②酸度对钒和铝的溶解量的影响如下图所示: 酸浸时溶液的酸度控制在大约3.2%,根据右图推测,酸浸时不选择更高酸度的原因是

(3)转沉:将浸出液中的钒转化为NH4VO3固体,其流程如下:

①浸出液中加入石灰乳的作用是
②已知CaCO3的溶解度小于Ca3(VO4)2。向Ca3(VO4)2沉淀中加入(NH4)2CO3溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:
③向(NH4)3VO4溶液中加入NH4Cl溶液,控制溶液的pH=7.5。当pH>8时,NH4VO3的产量明显降低,原因是
(4)测定产品中V2O5的纯度:称取ag产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1mL c1mol·L−1(NH4)2Fe(SO4)2溶液(VO2++2H++Fe2+=VO2++Fe3++H2O)。最后用c2mol·L−1KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2mL。已知MnO4−被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网