计算题 适中0.65 引用6 组卷346
CO、 、
、 是工业上重要的化工原料。
是工业上重要的化工原料。
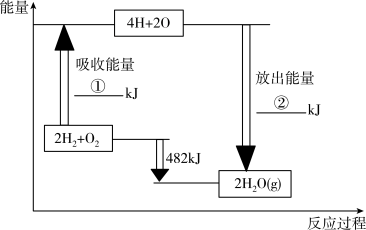
已知:①

②

③

请回答下列问题:
(1)上述反应中属于放热反应的是_______ (填标号)。
(2) 完全燃烧放出的热量为
完全燃烧放出的热量为_______ 。
(3)表示 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为_______ 。
(4)1.5mol由CO和 组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、
组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、 的物质的量分别为
的物质的量分别为_______ mol、_______ mol。
(5)等质量的 、
、 、
、 完全燃烧,放热最多的是
完全燃烧,放热最多的是_______ (填化学式)。
(6)某些常见化学键的键能数据如下表:
则

_______  。
。
已知:①
②
③
请回答下列问题:
(1)上述反应中属于放热反应的是
(2)
(3)表示
(4)1.5mol由CO和
(5)等质量的
(6)某些常见化学键的键能数据如下表:
| 化学键 | C=O | H—O | H—H | |
| 键能 | 803 | 463 | 436 | 1076 |
22-23高二上·新疆·期中
知识点:表示燃烧热的热化学方程式书写盖斯定律与热化学方程式依据热化学方程式的计算根据△H=反应物的键能之和-生成物的键能之和进行计算 答案解析 【答案】很抱歉,登录后才可免费查看答案和解析! 立即登录
类题推荐
甲醇既是重要的化工原料,又可作为燃料,还可以作为燃料电池的原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1 (已知:CO的结构与N2相似)
CH3OH(g) ΔH1 (已知:CO的结构与N2相似)
②CO2(g)+3H2(g) CH3OH(g)+H2O(g)ΔH2
CH3OH(g)+H2O(g)ΔH2
③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
由此计算ΔH1=______ kJ·mol-1,已知ΔH2=-58kJ·mol-1,则ΔH3=_____ kJ·mol-1。
(2)已知:
若甲醇的燃烧热为ΔH3,试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g) CH3OH(l)的ΔH=
CH3OH(l)的ΔH=________ 。若ΔH1=-285.8 kJ·mol-1,ΔH2=+283.0 kJ·mol-1,某H2和CO的混合气体完全燃烧时放出113.74 kJ热量,同时生成3.6g液态水,则原混合气体中H2和CO的物质的量之比为______ 。
(3)以CH4和H2O为原料,通过下列反应也可以制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)= =CH3OH (g)ΔH=-129.0 kJ·mol-1
CH4(g)+H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为__________ .
①CO(g)+2H2(g)
 CH3OH(g) ΔH1 (已知:CO的结构与N2相似)
CH3OH(g) ΔH1 (已知:CO的结构与N2相似)②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)ΔH2
CH3OH(g)+H2O(g)ΔH2③CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3回答下列问题:
(1)已知反应①中相关的化学键键能数据如下:
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(KJ/mol) | 436 | 343 | 1076 | 465 | 413 |
由此计算ΔH1=
(2)已知:
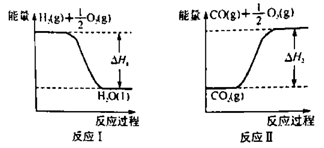
若甲醇的燃烧热为ΔH3,试用ΔH1、ΔH2、ΔH3表示CO(g)+2H2(g)
 CH3OH(l)的ΔH=
CH3OH(l)的ΔH=(3)以CH4和H2O为原料,通过下列反应也可以制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)= =CH3OH (g)ΔH=-129.0 kJ·mol-1
CH4(g)+H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网