解答题-原理综合题 适中0.65 引用2 组卷106
二氧化钛(TiO2)是一种重要的工业原料,可用四氯化钛(TiCl4)制备。已知:
I.TiCl4(g)+O2(g) TiO2(s)+2Cl2(g) △H1=-178.4kJ∙mol-1
TiO2(s)+2Cl2(g) △H1=-178.4kJ∙mol-1
II.2C(s)+O2(g) 2CO(g) △H2=-219.9kJ∙mol-1
2CO(g) △H2=-219.9kJ∙mol-1
请回答下列问题:
(1)TiCl4(g)与CO(g)反应生成TiO2(s)、C(s)和氯气的热化学方程式为____ 。
(2)若反应I的逆反应活化能表示为EkJ∙mol-1,则E____ 178.4(填“>”“<”或“=”)。
(3)t℃时,向10L恒容密闭容器中充入1molTiCl4和2molO2,发生反应I。4min达到平衡时测得TiO2的物质的量为0.2mol。
①0~4min内,用Cl2表示的反应速率v(Cl2)=_____ 。
②TiCl4的平衡转化率α=____ 。
③下列措施,既能加快反应速率又能增大TiCl4平衡转化率的是______ (填选项字母)。
A.缩小容器容积 B.加入催化剂 C.分离出部分TiO2 D.增大O2浓度 E.降低温度
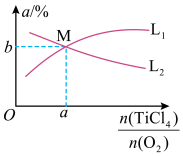
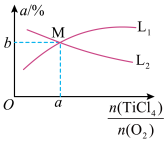
(4)t℃时,向10L恒容密闭容器中充入4molTiCl4和一定量O2的混合气体,发生反应I,两种气体的平衡转化率(α)与起始的物质的量之比[ ]的关系如图所示:能表示TiCl4平衡转化率的曲线为
]的关系如图所示:能表示TiCl4平衡转化率的曲线为______ (填“L1”或“L2”);M点的坐标为_____ 。
I.TiCl4(g)+O2(g)
II.2C(s)+O2(g)
请回答下列问题:
(1)TiCl4(g)与CO(g)反应生成TiO2(s)、C(s)和氯气的热化学方程式为
(2)若反应I的逆反应活化能表示为EkJ∙mol-1,则E
(3)t℃时,向10L恒容密闭容器中充入1molTiCl4和2molO2,发生反应I。4min达到平衡时测得TiO2的物质的量为0.2mol。
①0~4min内,用Cl2表示的反应速率v(Cl2)=
②TiCl4的平衡转化率α=
③下列措施,既能加快反应速率又能增大TiCl4平衡转化率的是
A.缩小容器容积 B.加入催化剂 C.分离出部分TiO2 D.增大O2浓度 E.降低温度
(4)t℃时,向10L恒容密闭容器中充入4molTiCl4和一定量O2的混合气体,发生反应I,两种气体的平衡转化率(α)与起始的物质的量之比[

22-23高二上·广东惠州·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网