解答题-实验探究题 适中0.65 引用1 组卷155
Na2O2是一种重要的氧化剂与供氧剂。
(一)研究Na2O2与水的反应。取一定量Na2O2,加入足量的水,充分反应。
(1)Na2O2的电子式是____ ;反应的化学方程式是____ 。
(2)收集并测量生成O2的体积,发现体积小于理论计算值。某小组研究产生这一差异的原因,进行如下实验。
查阅资料:
a.过氧化钠与水反应的过程中还可能存在以下两个复分解反应:
i.Na2O2+2H2O=2NaOH+H2O2
ii.Na2O2+H2O=NaOH+NaHO2
b.与H2O2类似,NaHO2也能在MnO2催化的条件下分解生成O2
2NaHO2 2NaOH+O2↑
2NaOH+O2↑
MnO2催化H2O2分解的化学方程式是____ 。
②依据资料设计如下实验:取0.02molNa2O2与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量MnO2,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化图所示。
已知:溶液中c(OH-)越大,溶液pH越大
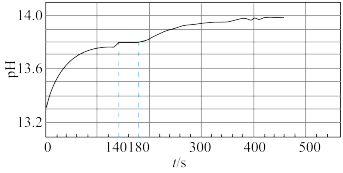
①小组同学根据pH的变化判断反应过程中一定发生反应ii,判断的理由是____ 。
根据140s-180s的pH计算出溶液的c(OH-)为0.6mol/L,则此时段内溶液中n(NaHO2)为____ 。
③由上述实验得出的结论是____ 。
(二)Na2O2空气中容易变质。某小组结合(一)的研究设计如下实验测定某久置的Na2O2的纯度。
向反应容器中加入一定质量的样品,____,再加入足量的水,收集产生的气体并测量体积(折合到标准状况),计算过氧化钠的纯度。
(3)补全上述实验方案____ 。
(4)与水类似,硫酸也能与过氧化钠发生类似反应,若用过量硫酸溶液替代上述方案中的一定量的水,其他测定条件不变,则测量结果会____ (填“偏大”、“偏小”或“不变”)。
(一)研究Na2O2与水的反应。取一定量Na2O2,加入足量的水,充分反应。
(1)Na2O2的电子式是
(2)收集并测量生成O2的体积,发现体积小于理论计算值。某小组研究产生这一差异的原因,进行如下实验。
查阅资料:
a.过氧化钠与水反应的过程中还可能存在以下两个复分解反应:
i.Na2O2+2H2O=2NaOH+H2O2
ii.Na2O2+H2O=NaOH+NaHO2
b.与H2O2类似,NaHO2也能在MnO2催化的条件下分解生成O2
2NaHO2
MnO2催化H2O2分解的化学方程式是
②依据资料设计如下实验:取0.02molNa2O2与足量水反应,140s时不再产生气泡,180s时向所得溶液中加入少量MnO2,立即产生无色气体。过程中溶液的体积始终约为40mL。反应过程中pH变化图所示。
已知:溶液中c(OH-)越大,溶液pH越大

①小组同学根据pH的变化判断反应过程中一定发生反应ii,判断的理由是
根据140s-180s的pH计算出溶液的c(OH-)为0.6mol/L,则此时段内溶液中n(NaHO2)为
③由上述实验得出的结论是
(二)Na2O2空气中容易变质。某小组结合(一)的研究设计如下实验测定某久置的Na2O2的纯度。
向反应容器中加入一定质量的样品,____,再加入足量的水,收集产生的气体并测量体积(折合到标准状况),计算过氧化钠的纯度。
(3)补全上述实验方案
(4)与水类似,硫酸也能与过氧化钠发生类似反应,若用过量硫酸溶液替代上述方案中的一定量的水,其他测定条件不变,则测量结果会
22-23高一上·北京西城·期中
类题推荐
某化学小组通过测量 粗品与水反应产生
粗品与水反应产生 的体积确定
的体积确定 的变质程度,但有资料显示
的变质程度,但有资料显示 与水反应收集到
与水反应收集到 的体积小于理论值。该小组查阅资料发现:
的体积小于理论值。该小组查阅资料发现:
a. 与水反应的过程中还可能存在以下两个复分解反应:
与水反应的过程中还可能存在以下两个复分解反应:
ⅰ.
ⅱ.
b. 能在
能在 催化的条件下分解生成
催化的条件下分解生成
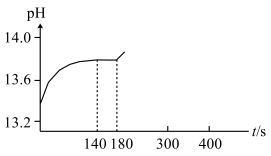
设计如下实验:取0.02 mol纯净 与足量水反应,140 s时不再产生气泡,180 s时向所得溶液中加入少量
与足量水反应,140 s时不再产生气泡,180 s时向所得溶液中加入少量 ,立即产生无色气体。过程中溶液的体积始终约为40 mL。反应过程中pH变化如图所示。
,立即产生无色气体。过程中溶液的体积始终约为40 mL。反应过程中pH变化如图所示。
下列说法错误的是
a.
ⅰ.
ⅱ.
b.
设计如下实验:取0.02 mol纯净

下列说法错误的是
| A.根据pH的变化可判断反应过程中一定发生反应ⅱ |
| B.若将 |
| C.140s~180s时,溶液中 |
| D.向8.0 g |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网