填空题 适中0.65 引用1 组卷76
化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_______(填字母)。
(2)向 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为
的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为 、
、 、
、 ,则三者由大到小的顺序为
,则三者由大到小的顺序为_______ 。
(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。
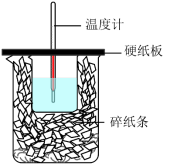
从实验装置上看,图中缺少的一种玻璃仪器是_______ 。若大烧杯上不盖硬纸板,求得的中和反应反应热
_______ (填“偏大”“偏小”或“无影响”)。
(4)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得:2H2(g)+O2(g)=2H2O(g) ΔH=_______ 。
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应ΔH=_______ 。
(5)硝酸厂的尾气直接排放将污染空气,日前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为

则甲烷直接将 还原为
还原为 的热化学方程式为
的热化学方程式为_______ 。
(1)下列反应中,属于放热反应的是_______(填字母)。
| A.碳与水蒸气反应 | B.铝和氧化铁反应 |
| C.CaCO3受热分解 | D.锌与盐酸反应 |
(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。

从实验装置上看,图中缺少的一种玻璃仪器是
(4)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 | H-H | O=O | O-H |
| 键能/kJ·mol-1 | 436 | 496 | 463.4 |
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应ΔH=
(5)硝酸厂的尾气直接排放将污染空气,日前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为
则甲烷直接将
22-23高二上·甘肃金昌·阶段练习
类题推荐
化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于吸热反应的是______ (填字母)。
A.Na2O与水反应 B.甲烷的燃烧反应 C.CaCO3受热分解 D.锌与盐酸反应
(2)获取能量变化的途径
① 通过化学键的键能计算。已知:
计算可得:2H2(g)+ O2(g) =2H2O(g) ∆H=____________ kJ·mol-1
② 通过物质所含能量计算。已知反应中A+B=C+D中A、B、C、D所含能量依次可表示为E A、EB、 EC、 ED,该反应△H=_______ 。
③ 通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+ O2 (g) =Na2O(s) △H=-414kJ·mol-1
O2 (g) =Na2O(s) △H=-414kJ·mol-1
Ⅱ.2Na(s)+O2(g) =Na2O2(s) △H=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式__________ 。
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入________ (填序号)。
A.50 mL 0.50 mol·L-1 NaOH溶液
B.50 mL 0.55 mol·L-1NaOH溶液
C.1.0 g NaOH固体
(1)下列反应中,属于吸热反应的是
A.Na2O与水反应 B.甲烷的燃烧反应 C.CaCO3受热分解 D.锌与盐酸反应
(2)获取能量变化的途径
① 通过化学键的键能计算。已知:
| 化学键种类 | H—H | O=O | O—H |
| 键能(kJ/mol) | 436 | 498 | 463.4 |
计算可得:2H2(g)+ O2(g) =2H2O(g) ∆H=
② 通过物质所含能量计算。已知反应中A+B=C+D中A、B、C、D所含能量依次可表示为E A、EB、 EC、 ED,该反应△H=
③ 通过盖斯定律可计算。已知在25℃、101kPa时:
Ⅰ.2Na(s)+
Ⅱ.2Na(s)+O2(g) =Na2O2(s) △H=-511kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式
④利用实验装置测量。测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入
A.50 mL 0.50 mol·L-1 NaOH溶液
B.50 mL 0.55 mol·L-1NaOH溶液
C.1.0 g NaOH固体
化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_________ (填字母)。
A. 碳与水蒸气反应 B .铝和氧化铁反应 C .CaCO3受热分解 D .锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得:2H2(g)+O2(g)=2H2O(g) △H=____ 。
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应△H=______ 。
③通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+ O2(g)=Na2O(s) △H=-412 kJ·mol-1
O2(g)=Na2O(s) △H=-412 kJ·mol-1
II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式_______________ 。
④利用实验装置测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入________ (填序号)。
A .1.0 g NaOH固体 B. 50 mL 0.50 mol·L-1 NaOH溶液 C .50 mL0.55 mol·L-1 NaOH溶液
(1)下列反应中,属于放热反应的是
A. 碳与水蒸气反应 B .铝和氧化铁反应 C .CaCO3受热分解 D .锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 | H-H | O=O | O-H |
| 键能(kJ/ mol) | 436 | 496 | 463.4 |
计算可得:2H2(g)+O2(g)=2H2O(g) △H=
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应△H=
③通过盖斯定律可计算。已知在25℃、101 kPa时:
I.2Na(s)+
II.2Na(s)+O2(g)=Na2O2(s) △H=-511 kJ·mol-1
写出Na2O2与Na反应生成Na2O的热化学方程式
④利用实验装置测量盐酸与NaOH溶液反应的热量变化的过程中,若取50 mL 0.50 mol·L-1的盐酸,则还需加入
A .1.0 g NaOH固体 B. 50 mL 0.50 mol·L-1 NaOH溶液 C .50 mL0.55 mol·L-1 NaOH溶液
回答下列问题:
(1)实验测得10g液态甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出227kJ的热量。试写出甲醇燃烧的热化学方程式:_____ 。
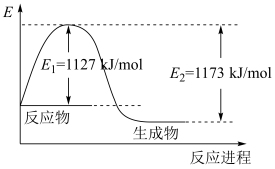
(2)现已知A2(g)和B2(g)反应生成1 molAB3(g)过程中能量变化示意如下图。根据下列已知键能数据计算A-B键键能为___________ kJ/mol。
(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
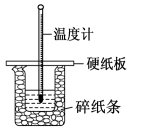
①从实验装置上看,图中缺少的一种玻璃仪器是___________ 。烧杯间填满碎纸条的作用是___________ 。若大烧杯上不盖硬纸板,求得的中和热ΔH___________ (填“偏大”“偏小”或“无影响”)。
②甲同学用50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行中和反应,通过计算得到ΔH=-54.8kJ/mol,该结果与ΔH=-57.3kJ·mol-1有偏差,产生此偏差的原因可能是___________ 。
A、用温度计测定HCl溶液起始温度后直接测定NaOH溶液的温度
B、一次性把NaOH溶液倒入盛有硫酸的小烧杯中
C.实验装置保温、隔热效果差
③若改用60 mL 0.50 mol·L-1盐酸与60 mL 0.55 mol·L-1NaOH溶液进行反应,两个实验相比,所放出的热量___________ (填“相等”或“不相等”),所求中和热___________ (填“相等”或“不相等”)若用50mL0.5mol·L-1醋酸代替盐酸溶液进行上述实验,测得反应前后温度的变化值会___________ (填“偏大”、“偏小”或“不受影响”)。
(1)实验测得10g液态甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出227kJ的热量。试写出甲醇燃烧的热化学方程式:
(2)现已知A2(g)和B2(g)反应生成1 molAB3(g)过程中能量变化示意如下图。根据下列已知键能数据计算A-B键键能为

| 化学键 | A≡A | B-B |
| 键能(kJ/mol) | 946 | 436 |
(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:

①从实验装置上看,图中缺少的一种玻璃仪器是
②甲同学用50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液进行中和反应,通过计算得到ΔH=-54.8kJ/mol,该结果与ΔH=-57.3kJ·mol-1有偏差,产生此偏差的原因可能是
A、用温度计测定HCl溶液起始温度后直接测定NaOH溶液的温度
B、一次性把NaOH溶液倒入盛有硫酸的小烧杯中
C.实验装置保温、隔热效果差
③若改用60 mL 0.50 mol·L-1盐酸与60 mL 0.55 mol·L-1NaOH溶液进行反应,两个实验相比,所放出的热量
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


