填空题 较易0.85 引用1 组卷91
某实验小组欲探究影响化学反应速率的因素,设计实验方案如下:
利用 和
和 (草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用
(草酸)在酸性溶液中发生氧化还原反应来探究化学反应速率的影响因素(实验中所用 溶液已加入稀硫酸酸化)
溶液已加入稀硫酸酸化)
(1)用离子方程式表示该反应的原理:_______
实验设计方案如下:
(2)该实验探究的是_______ 对化学反应速率的影响。褪色时间由小到大的顺序是_______ (填实验序号)。
(3)实验①测得 溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
溶液的褪色时间为10min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率
_______  。
。
利用
(1)用离子方程式表示该反应的原理:
实验设计方案如下:
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/L | 3mL 0.01mol/L |
| ② | 2mL 0.2mol/L | 3mL 0.01mol/ L |
| ③ | 2mL 0.2mol/L | 3mL 0.01mol/L |
(3)实验①测得
22-23高二上·广东佛山·阶段练习
类题推荐
甲、乙、丙三个实验小组欲探究影响化学反应速率的因素,设计实验方案如下:
I.甲组:利用KMnO4和H2C2O4(草酸)在酸性溶液中发生氧化还原反应生成CO2气体体积来探究化学反应速率的影响因素(实验中所用KMnO4溶液已加入稀硫酸酸化)。
(1)用离子方程式表示该反应的原理:_____ 。
实验装置如图所示,实验时分液漏斗中A溶液一次性加入,A、B的成分见下表:

(2)该实验装置检查气密性的方法是_____ 。
(3)该实验探究的是___________ 对化学反应速率的影响。在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序是___________ (填实验序号)。
II.乙组:通过测定KMnO4和H2C2O4(草酸)在酸性溶液中发生反应时KMnO4溶液褪色所需时间的长短探究浓度对化学反应速率的影响。该实验小组配制了以下溶液:①0.01 mol/L KMnO4溶液2 mL;②0.20 mol/L KMnO4溶液2 mL;③0.10 mol/L H2C2O4溶液6 mL;④0.20 mol/L H2C2O4溶液6 mL。
(4)实验时使用下列各组试剂中合理的一组是___________(填字母)。
(5)使用上面选择那组试剂进行实验,测得溶液褪色时间分别为10s和5 s,计算褪色时间为10s的实验中草酸的反应速率v(H2C2O4)=___________ mol/(L·s)。
I.甲组:利用KMnO4和H2C2O4(草酸)在酸性溶液中发生氧化还原反应生成CO2气体体积来探究化学反应速率的影响因素(实验中所用KMnO4溶液已加入稀硫酸酸化)。
(1)用离子方程式表示该反应的原理:
实验装置如图所示,实验时分液漏斗中A溶液一次性加入,A、B的成分见下表:

| 序号 | A溶液 | B溶液 |
| ① | 2 mL 0.1 mol/LH2C2O4 (aq) | 4 mL 0.01 mol/L KMnO4(aq) |
| ② | 2 mL 0. 2 mol/LH2C2O4 (aq) | 4 mL 0.01 mol/L KMnO4(aq) |
| ③ | 2 mL 0. 2 mol/LH2C2O4 (aq) | 4 mL 0.01 mol/L KMnO4(aq) + MnSO4(少量) |
(3)该实验探究的是
II.乙组:通过测定KMnO4和H2C2O4(草酸)在酸性溶液中发生反应时KMnO4溶液褪色所需时间的长短探究浓度对化学反应速率的影响。该实验小组配制了以下溶液:①0.01 mol/L KMnO4溶液2 mL;②0.20 mol/L KMnO4溶液2 mL;③0.10 mol/L H2C2O4溶液6 mL;④0.20 mol/L H2C2O4溶液6 mL。
(4)实验时使用下列各组试剂中合理的一组是___________(填字母)。
| A.①②③ | B.①②④ | C.①③④ | D.②③④ |
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素。
(1)该反应的离子方程式为__________________________ 。
设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
(2)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:
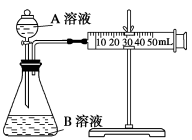
该实验探究的是______ 对化学反应速率的影响。在反应停止之前,相同时间内针管中所得CO2的体积由大到小的顺序是____________ (用实验序号填空)。
(3)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小。取两支试管各加入2 mL 0.1 mol/L H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol/L KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验目的是研究_________ 对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是____________ 。
(1)该反应的离子方程式为
设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
(2)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小。实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见下表:

| 序号 | A溶液 | B溶液 |
| ① | 2 mL 0.1 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ② | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ③ | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液和少量MnSO4 |
(3)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小。取两支试管各加入2 mL 0.1 mol/L H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol/L KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验目的是研究
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该反应的离子方程式___________________________ 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是_____________ 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_________________ <_____________ (填实验序号)。
(3)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末, c( )=
)=__________ mol/L(假设混合液体积为50mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定_____________ 来比较化学反应速率。(一条即可)
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

①__________________________ ;②__________________________ 。
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1 H2C2O4溶液 | 30mL 0.01mol·L-1 KMnO4溶液 |
| ② | 20mL 0.2mol·L-1 H2C2O4溶液 | 30mL 0.01mol·L-1 KMnO4溶液 |
(1)该反应的离子方程式
(2)该实验探究的是
(3)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末, c(
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

①
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


