解答题-结构与性质 较难0.4 引用1 组卷329
硼、铝元素位于金属分界线附近,其化合物性质相对复杂。
(1)硼在元素周期表中的位置是___________ 。铍、硼、铝的第一电离能从大到小依次是___________ 。
(2) 分子的空间形状为
分子的空间形状为___________ ,B原子的杂化形式为___________ 。
(3) 可与
可与 溶液反应得到
溶液反应得到 溶液。结晶可得
溶液。结晶可得 晶体,其熔点为
晶体,其熔点为 ,由
,由 构成。
构成。 的结构式为
的结构式为___________ 。(已知: 的结构式为
的结构式为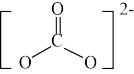 )
)
(4) 的晶体结构与
的晶体结构与 相似,其熔点为
相似,其熔点为 。请解释其熔点小于
。请解释其熔点小于 的原因:原子半径:
的原因:原子半径: ,
,___________ 。
(5)研究表明:NaAlCl4化学性质较为稳定,加热至 以上才开始分解,得到
以上才开始分解,得到 。而
。而 在
在 即开始分解,释放出
即开始分解,释放出 。已知:
。已知:
ⅰ.这两种物质的稳定性主要与阴离子的配位键强弱有关,其他因素影响较小;
ⅱ.配位键键能与中心原子接受电子的能力、配位原子给出电子的能力有关。
请从原子结构角度解释两种物质的稳定性差异:两种物质的阴离子中心原子相同,配位原子不同;F与 原子最外层电子数相同,电子层数:
原子最外层电子数相同,电子层数: ,原子半径:
,原子半径: ,
,___________ ,稳定性: 。
。
(1)硼在元素周期表中的位置是
(2)
(3)
 )
)(4)
(5)研究表明:NaAlCl4化学性质较为稳定,加热至
ⅰ.这两种物质的稳定性主要与阴离子的配位键强弱有关,其他因素影响较小;
ⅱ.配位键键能与中心原子接受电子的能力、配位原子给出电子的能力有关。
请从原子结构角度解释两种物质的稳定性差异:两种物质的阴离子中心原子相同,配位原子不同;F与
22-23高三上·北京海淀·期中
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网




