解答题-原理综合题 适中0.65 引用1 组卷95
铁及其化合物在日常生活和生产中有广泛的应用。
(1)防止钢铁腐蚀造成浪费是科学家很关心的一个话题。
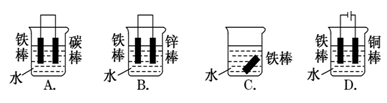
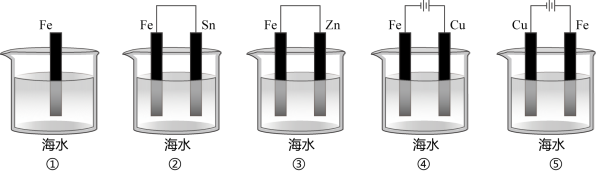
①下列各情况,其中Fe片腐蚀由快到慢的顺序是(用序号表示)_______ 。
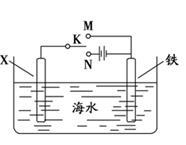
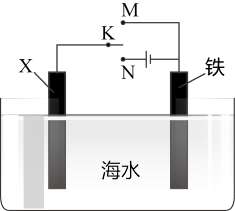
②利用如图装置,可以模拟铁的电化学防护,若X为碳棒,为减缓铁的腐蚀,开关K应设置于_______ 处。若X为锌,开关K置于M处,该电化学防护法称为_______ 。
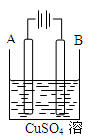
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:
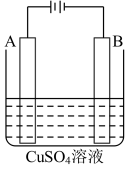
A电极对应的金属是_______ (写元素名称),B电极的电极反应式是_______ 。
(3) 是一种高效多功能水处理剂,应用前景非常看好,电解法制取原理如图所示,装置通电后,铁电极附近生成紫红色的
是一种高效多功能水处理剂,应用前景非常看好,电解法制取原理如图所示,装置通电后,铁电极附近生成紫红色的 ,镍电极有气泡产生。
,镍电极有气泡产生。

①离子交换膜为阴离子交换膜,阴极室中NaOH的浓度_______ (填写“变大”、“变小”或“不变”)
②阳极室中电极反应式是_______ 。
(4) (二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为
(二硫化亚铁)纳米材料,该材料可用于制造高容量锂电池,电池放电时的总反应为 ,正极反应式是
,正极反应式是_______ 。
(1)防止钢铁腐蚀造成浪费是科学家很关心的一个话题。
①下列各情况,其中Fe片腐蚀由快到慢的顺序是(用序号表示)

②利用如图装置,可以模拟铁的电化学防护,若X为碳棒,为减缓铁的腐蚀,开关K应设置于

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

A电极对应的金属是
(3)

①离子交换膜为阴离子交换膜,阴极室中NaOH的浓度
②阳极室中电极反应式是
(4)
22-23高二上·广西河池·阶段练习
类题推荐
物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。请根据所学知识回答下列问题:
(1)在25℃,将一元酸HA的溶液和KOH溶液等体积混合(忽略反应后溶液的体积变化),其实验数据如下表:
①实验1中反应后的溶液中各离子浓度由大到小关系为:___________ 。
②实验2反应后的溶液中:c(A-)+c(HA)_______ 0.2mol/L (填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(2)实验室中配制 溶液时通常需向其中加入盐酸,其目的是
溶液时通常需向其中加入盐酸,其目的是___________ ,实验测得 溶液的
溶液的 ,某同学将
,某同学将 溶液和
溶液和 溶液混合在一起,发现产生了红褐色沉淀和无色气体,该反应的离子方程式为:
溶液混合在一起,发现产生了红褐色沉淀和无色气体,该反应的离子方程式为:___________ 。
(3)某温度时, ,
, ,
, 。某溶液含有
。某溶液含有 、
、 和
和 ,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的
,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的 溶液,三种阴离子产生沉淀的先后顺序为
溶液,三种阴离子产生沉淀的先后顺序为___________ (用阴离子符号表示)。
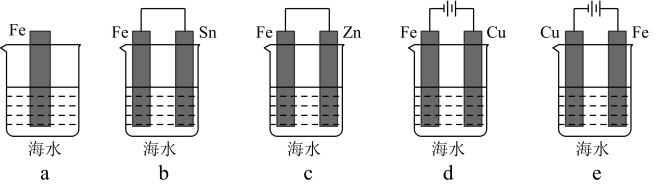
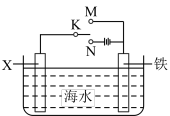
(4)利用如图装置可以模拟铁的电化学防护。
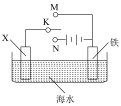
①若X为碳棒,为减缓铁的腐蚀,开关K应置于_____ 处。假设海水中只有NaCl溶质,写出此时总离子反应方程式:_____ 。
②若X为锌,开关K置于M处,该电化学防护法称为_____ ,写出铁电极处的电极反应式:_____ 。
(1)在25℃,将一元酸HA的溶液和KOH溶液等体积混合(忽略反应后溶液的体积变化),其实验数据如下表:
实验编号 | 起始浓度/(mol/L) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
1 | 0.2 | 0.2 | |
2 | 0.4 | ||
②实验2反应后的溶液中:c(A-)+c(HA)
(2)实验室中配制
(3)某温度时,
(4)利用如图装置可以模拟铁的电化学防护。

①若X为碳棒,为减缓铁的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网